«Зомби-клетки» внутри нас
В вашем теле живут клетки-зомби. Они не совсем мёртвые. Такие клетки скорее живые, но они больше не делятся и могут свою «зомби-сущность» передавать соседям. И соседние клетки тоже превращаются в зомби! Зомби-клетки повышают риск рака и разных других заболеваний — например, артеросклероза. Сейчас учёные активно думают о том, как от таких клеток избавиться. Однако есть нюанс: наши внутренние «зомби» выполняют и полезные функции.
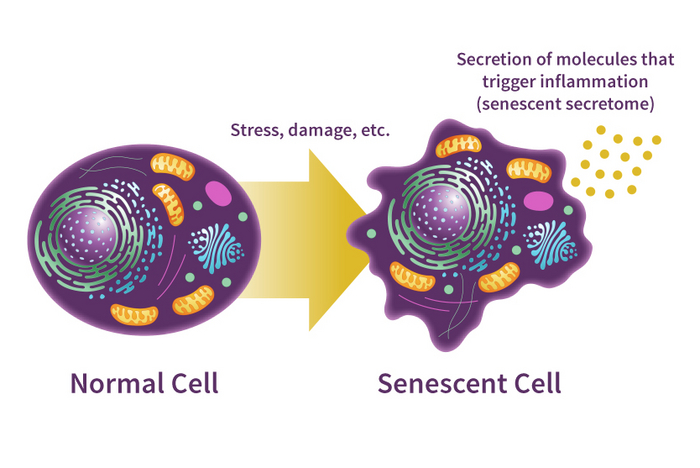
Учёные называют «зомби» сенесцентными клетками. И накопление этого типа клеток в нашем организме — очень важный элемент человеческого старения. Говоря простым языком, сенесцентные клетки — это клетки, которые ранее обладали способностью делиться, но из-за накопления разных повреждений делиться больше не могут. Обычно количество «зомби» с возрастом увеличивается. Из-за этого появляются разные старческие заболевания, возникает боль в суставах, нарушения когнитивных функций, системные воспаления и так далее.
Откуда в нашем теле берутся сенесцентные клетки? Это точно не старые клетки — некоторые «зомби» образуются ещё на стадии эмбрионального развития. Чаще всего сенесцентные клетки, вызывающие заболевания, появляются из-за ошибок, мутаций в ДНК и иных повреждений. Клетка, в которой накопилось много повреждений, выходит из клеточного цикла и как бы говорит: «Всё, я дальше делиться не буду». А ещё «зомби» сигнализируют о своём состоянии иммунной системе, выбрасывая провоспалительные факторы. На эти факторы «приходит» иммунная система и некоторые сенесцентные клетки утилизирует.
Ещё «зомби» могут образовываться из-за повышенной активности отдельных генов. Например, когда клетка подозревает, что может стать раковой, она превращается в сенесцентную. И это хорошо! А сейчас приведу пример, который всем понятен — родинки. Наверняка мои читатели слышали про меланому — рак кожи. Родинки — это не меланома, но в родинках клетки начинают очень активно делиться. Затем в них включается механизм сенесценции — и они делиться перестают. И родинка оказывается «зафиксированной» в своём размере и не превращается в раковую опухоль.
Важно сказать, что сенесцентные клетки могут быть очень разными как по происхождению, так и по свойствам. Поэтому некоторые учёные очень скептично относятся к термину «сенесцентные клетки» — ведь не всегда понятно, какие именно клетки имеются в виду. Интуитивно может показаться, что, раз клетка перестала делиться, значит, в ней что-то сломалось. Но на самом деле «зомби» — это клетки, в которых сработал специальный и целенаправленный механизм, который ограничивает клеточное деление. Так задумано — это не случайная поломка. Это, скорее всего, специальная «поломка» ради предотвращения онкологического заболевания.
Когда клетка сильно повреждается и не может эти повреждения исправить, у неё есть две опции. Первая — запрограммированная клеточная смерть, самоубийство клетки или апоптоз. Вторая — превращение в «зомби». Во втором случае клетка выживает, но перестаёт делиться.
Перед тем как выбрать одну из двух опций клетка пытается себя починить. Когда в клетке повреждается ДНК, включается огромное количество механизмов «репарации». Активируются разные белки, которые пытаются это дело исправить. Однако, если ошибку устранить не получается, клетке приходится выбирать одну из двух упомянутых опций.
Существует по меньшей мере четыре вида сенесценции:
Репликативное старение. У большинства клеток есть встроенный ограничитель делений — предел Хейфлика. При каждом делении кончики хромосом — теломеры — укорачиваются. И через 40-60 делений клетка перестаёт делиться — это и есть репликативное старение. Это старение особенно распространено у крупных видов животных — в частности, у человека;
Сенестенция, вызванная стрессом. Здесь речь идёт не о депрессии, а о том, что клетка может повреждаться из-за ультрафиолетового излучения, ионизирующей радиации, активных форм кислорода и так далее. В результате клетка перестаёт делиться;
Сенесценция, вызванная онкогенами. Онкогены — это гены, чья повышенная активность увеличивает риск рака. Если клетка «замечает» онкогены, то перестаёт делиться;
Сенесценция эмбрионального развития. У человека есть разные эмбриональные структуры, которые не должны чересчур разрастись в утробе. А некоторые структуры даже должны исчезнуть совсем — например, плавники и хвостик у зародыша. Благодаря сенесцентному механизму младенцы появляются на свет без хвоста!
В общем, сенесценция — это довольно нужно и важно. И всё же есть учёные, которые называют сенесцентные клетки «зомби» и считают, что от некоторых из них нужно избавляться — чтобы победить старение.
Итак, у сенесценции есть плюсы и минусы. Сначала расскажу о плюсах. Благодаря «зомби» организм предотвращает появление некоторых онкологических заболеваний. Учёные создавали ГМ-животных с отключенным геном p16. p16 — один из ключевых генов, запускающих сенесцентность. В результате подопытные массово страдали от рака. То есть полностью сенесценцию отключать нельзя! Кроме того, учёные выяснили, что «зомби» иногда помогают регенерировать ткани кожи и мышц. А сенесценция клеток поджелудочной железы может увеличивать выработку инсулина. Сенесценция же клеток печени предотвращает цирроз. В общем, «зомби» делают массу всего полезного. Кстати, такие «зомби» встречаются даже у сверхдолгожителей — голых землекопов.
При этом сенесцентные клетки обладают и рядом «недостатков». Так, с возрастом в нашем теле накапливается очень много «зомби». Особенно опасны клетки, ставшие «зомби» из-за повреждений в ДНК. Они начинают производить молекулы, которые могут вызывать хронические воспаления в тканях вокруг. Так, есть очень важная провоспалительная молекула — интерлейкин-6. Она нужна для коммуникации клеток между собой. Интерлейкин-6 активирует высокую температуру при заболеваниях, влияет на исход некоторых видов рака... Когда клетки перестают делиться из-за сенесценции, порой они начинают производить в 40 раз больше интерлейкина-6. От этого могут повреждаться соседние клетки — и у них тоже включается сенесценция. Происходит цепная реакция.
И ещё один момент: в нашем теле есть «спящие» эндогенные вирусы, которые изначально встроены в наш геном. Они попали туда в ходе эволюции и зашифрованы прямо в нашей ДНК. Так вот, в норме особые клеточные механизмы подавляют вирусы и не дают им сделать ничего плохого. Однако, как показало недавнее исследование, «зомби» не подавляют такие эндогенные вирусы. И в итоге клетка собирает из своего же генома вирусные частицы и заражает ими здоровые клетки. Заражённые клетки, в свою очередь, тоже становятся сенесцентными. Но всё не так плохо: авторы упомянутого исследования создали антитела против вирусных частиц — и остановили заражение.
Но всё же сенесцентные клетки опасны в первую очередь из-за хронического воспаления, которое они вызывают. Инфекции в организме нет, а воспаление есть. И иммунитет борется, по сути, с самим организмом. В итоге из-за хронического системного воспаления возникают артрит, атеросклероз и прочие неприятные «старческие» заболевания. Иногда из-за воспаления возникает рак, деменция, болезнь почек, депрессия. А ещё выраженность системного хронического воспаления очень неплохо предсказывает вероятности смерти человека.
Откуда мы знаем, что сенесцентные клетки существуют и работают? Надо признать: есть учёные, которые скептически относятся к концепции сенесцентных клеток. Как минимум потому, что «зомби» трудно дать точное определение — уж очень разными они бывают. Но одна команда исследователей провела эксперимент, показавший «работоспособность» сенесцентных клеток. Итак, учёные взяли клетки эпителия в предраковом состоянии — в них уже «назрели» мутации, вызывающие рак. Потом эти предраковые клетки исследователи смешали либо с сенесцентными клетками, либо с обычными, несенесцентными, которые могут делиться. А дальше ввели и первую, и вторую смесь подопытным грызунам. Оказалось, что при введении смеси из предраковых и сенесцентных клеток повышается и риск появления рака, и скорость роста опухоли. А при введении другой смеси — с нормальными клетками — таких страшных последствий не наблюдалось.
Считается, что рак — это результат мутаций в клетках. Но на самом деле на успешность и активность раковой клетки влияют ещё и соседние клетки. И если рядом с потенциально мутантной раковой клеткой находятся сенесцентные клетки, шанс развития рака повышается.
Другая команда учёных поставила ещё один опыт — взяла свиные клетки и превратила часть из них с помощью радиации в сенесцентные. Затем и нормальные клетки, и «зомби» исследователи перенесли в почки молодых мышей. Выяснилось, что из-за сенесцентных клеток у грызунов начали возникать фиброзы, воспаления и различные повреждения почек. Похожий опыт провела ещё одна группа учёных: они брали из жировой ткани мышек как сенесцентные, так и нормальные клетки, которые способны делиться. Далее специалисты понемногу пересаживали клетки другим грызунам. Выяснилось, что мышки, которым подсаживали «зомби-клетки», начали проявлять признаки старения — они хуже бегали, становились слабее. Чем больше грызун получал сенесцентных клеток, тем дряхлее он становился. В ходе эксперимента учёные выяснили, что 1 сенесцентная клетка на 10 000 нормальных примерно в 5 раз увеличивает риск смерти.
Что же делать — избавляться от «зомби» или нет? Видимо, надо оставить механизм сенесценции в покое — но при этом можно устранять уже получившиеся «зомби» по мере их накопления. Как это сделать? Наши гены должны активироваться в определённых условиях. Поэтому у каждого гена есть регуляторный участок, который «говорит», где именно и в каких условиях ген будет работать (пример такого участка — промотор, который находится перед началом гена и показывает, с какого места его «считывать»). Так мы можем «подсмотреть», какие гены активируются в сенесцентных клетках. В общем, учёные выяснили, что у существенной части сенесцентных клеток их сенесцентность запускалась уже упомянутым геном p16. У p16, как и у любого другого гена, есть промотор — вот его-то и можно «приделать» к другому гену. Тогда при «запуске» p16 параллельно запустится и тот второй ген. А теперь фокус: приклеиваем промотор p16 к гену, который запускает запрограммированную смерть клетки! Тогда в момент, когда клетка по какой-то причине «решит» стать сенесцентной, она тут же себя и убьёт.
А можно пойти ещё более хитрым путём. Например, сделать так, чтобы наш дополнительный ген, к которому мы приклеили промотор от p16, срабатывал бы только при наличии синтетического вещества, которого не бывает в организме человека. То есть, когда мышке или человеку вводят это секретное вещество, все клетки, где активен p16, убьются. Так исчезнут клетки с повреждённой ДНК, которые больше не делятся. Но будет ли такая «зачистка» полезна для здоровья?
Учёные выяснили, что да, «зачистка» скорее полезна. Исследователи в ходе своего эксперимента удаляли сенесцентные клетки у ГМ-мышей — и продолжительность жизни грызунов немного выросла! При этом животные выглядели моложе сверстников и были более активными, любознательными и бодрыми. Это круто — получается, удаление сенесцентных клеток поможет в борьбе со старением.
Но, увы, такая генная терапия должна происходить до рождения — а мы с вами взрослые люди, нас в эмбриональное состояние уже не вернуть. Что же нам делать? Как избавиться от вредных клеток? Хорошие новости: уже разработаны препараты — сенолитики — которые могут уничтожить некоторые типы сенесцентных клеток. По крайней мере, так показали опыты на животных. Так вот, самая известная комбинация сенолитиков — это дазатиниб и кверцетин. Дазатиниб — это вообще лекарство от рака и опухолей. А кверцетин — это природное вещество, которое достаточно часто встречается в продуктах питания. Исследования показали, что кверцетин усиливает действие дазатиниба.
Я уже описывал эксперимент, авторы которого пересаживали мышам сенесцентные клетки из жировой ткани. Так вот, в той работе учёные брали клетки у ГМ-доноров со светящимися клетками. Клетки доноров отличались от клеток реципиентов, их можно было легко увидеть под микроскопом. В ходе опыта реципиентам давали дазатиниб и кверцетин — и выяснилось, что сенолитики устраняли светящихся «зомби», но не устраняли нормальные светящиеся клетки. А ещё учёные поставили дополнительный эксперимент на старых мышах, чей возраст примерно эквивалентентен возрасту 80-летних стариков. Им давали те же дазатиниб и кверцетин. «С момента лечения продолжительность жизни мышей увеличилась на 36%», — резюмировали авторы статьи. Но на самом деле старые мышки просто чуть-чуть дольше протянули.
Другие учёные показали, что дазатиниб и кверцетин замедляют старение лёгких у мышей. А ещё одни исследователи поставили эксперимент на людях — правда, людей было всего 9, то есть выборка оказалась ничтожно мала. Тем не менее, учёные заявили, что сенолитики снизили число «зомби» в тканях. А вот как препараты повлияли на продолжительность жизни, непонятно — люди, в отличие от мышей, слишком долго живут, на них такие эксперименты ставить сложно.
Кроме микса из дазатиниба и кверцетина, существуют и другие сенолитики. Например, популярен экспериментальный препарат навитоклакс — тоже средство против рака. Вы, наверное, спросите: как противоопухолевое лекарство от рака помогает против сенесцентных клеток? Ведь раковые клетки суперактивно делятся, а «зомби» не делятся вовсе. Но у этих двух типов клеток есть нечто общее — у них постоянно включены «сигналы об ошибке», о повреждениях. Правда, «зомби» в ответ на сигнал перестают делиться, а раковые клетки сигнал игнорируют и очень активно делятся.
В одной работе учёные исследовали сенесцентные клетки в сердцах грызунов. Да-да, в сердце тоже могут появляться «зомби» — это приводит к фиброзу и гипертрофии сердца, что увеличивает риск внезапной смерти. В общем, учёные вызывали инфаркт у мышей. И выяснили, что старые 23-месячные грызуны, которым ранее давали навитоклакс, выздоравливали после инфаркта как 3-месячные мышки. Это как если бы 70-летний старик отошёл от инфаркта как подросток.
К сожалению, у сенолитиков есть побочные эффекты — в частности, малоприятный кашель с кровью. А теперь — к хорошим новостям:
Для борьбы с «зомби» нужны не такие высокие дозировки, как для борьбы с раком;
Сенолитики можно принимать не постоянно, а курсами: попил, а потом дальше живёшь и «копишь» своих «зомби» лет 10-20;
Есть такой сенолитик — квертицин — который идёт в комбо с дазатинибом и почти не имеет побочек. Сам по себе это флавоноид, которого много в разных фруктах и овощах, особенно в каперсах. Правда, есть овощи ради кверцитина бесполезно: чтобы получить нужное количество вещества, придётся есть по полкило каперсов в день. Что делает кверцитин? Он подавляет белок, который не даёт клетке убить себя, говорит ей «Живи!» Грубо говоря, этот белок как психотерапевт. А кверцитин приходит и убивает психотерапевта, а клетка такая: «Всё, не хочу больше жить».
Сейчас много хайпа вокруг ещё одного сенолитика — физетина. Он тоже встречается в разных фруктах и овощах — в яблоках, огурцах, луке, винограде. Биохакеры очень любят кушать физетин! Но есть нюанс. Существует научная программа тестирования интервенций — Interventions Testing Program. Она беспристрастно испытывает всякие средства против старения — три разных лаборатории в США независимо тестируют предлагаемые способы на мышах, самцах и самках. В общем, согласно Interventions Testing Program, физетин жизнь не продлевает.
Но вообще, даже если физетин или другой сенолитик работает на мышах, это не значит, что он будет работать и на нас с вами. Из 100 препаратов, которые работают на грызунах, лишь 10 оказываются эффективными на людях. Так что ждём исследований сенолитиков на людях — чтобы понять, какие из них работают — и работают без серьёзных побочных эффектов.
У нас есть часть тела, где клетки вообще не делятся — это наш мозг. Да-да, нейроны делиться не умеют, а ещё они с годами могут ухудшаться и дряхлеть. У дряхлых нейронов может, например, уменьшаться объём митохондрий. А ещё стареющие нейроны могут выделять интерлейкин-6. А значит, вызывать старческое хроническое воспаление в мозге. То же самое может происходить и с клетками, которые питают и берегут нейроны — например, с астроцитами. И даже у стволовых клеток может случаться сентенция!
В общем, кажется, дела плохи: в нашем мозге, скорее всего, с возрастом настанет старческое хроническое воспаление. Кстати, были опыты, в ходе которых в мозг мышам вводили интерлейкин-6 — и это приводило к ухудшению когнитивных функций грызунов. А ещё учёные знают, что у пациентов с Паркинсоном и Альцгеймером в спинномозговой жидкости находится много противовоспалительных маркёров.
Учёные исследовали влияние сенолитиков на мозг мышей. Оказалось, что сенолитики могут избирательно устранять «сенесцентноподобные» нейроны — повреждённые нейроны, которые вызывают воспаления. И в итоге у грызунов после устранения «проблемных» нейронов улучшились когнитивные способности. Вывод тут простой: лучше потерять немного повреждённых нейронов сегодня, но предотвратить воспаление и сохранить гораздо большее количество здоровых нейронов завтра.
Но всё же пока учёные не знают точно, стоит ли избавляться от «зомби» с помощью лекарств, предназначенных для лечения рака. А ещё устранение сенесцентных клеток — не панацея от старости, ведь «зомби» — лишь один из симптомов этого неприятного процесса. У старения больше дюжины причин!
Тем не менее, обращать внимание на сенесцентные клетки важно, потому что они приводят к системным воспалениям, а такие воспаления — сильный предсказатель смертности у людей. Недаром есть исследование: у людей, которые прожили больше 110 лет, гораздо ниже уровни маркеров воспаления — таких как интерлейкин-6. И это не совпадение. Так что продолжаем изучать сенолитики!
Напоследок расскажу про недавние эксперименты на мушках-дрозофилах. Авторы работы решили объединить два метода продления жизни:
Они удаляли «зомби»;
А ещё омолаживали другие клетки организма с помощью факторов Яманаки, превращая их в стволовые — чтобы они активнее делились и восполняли удалённые дряхлые клетки.
Учёные пришли к выводу, что вместе эти два способа дали результат лучше, чем использование лишь одного метода. Это в очередной раз говорит о том, что старение — это множество разных процессов. И чтобы его победить, нужно использовать одновременно разные методы — чинить митохондрии, увеличивать число стволовых клеток и уменьшать число «зомби», удлинять теломеразу и устранять мутации. Думаю, в будущем возникнет комбинированная терапия против старения — и люди будут жить значительно дольше, чем сейчас.
Улучшить и создать с нуля — какие возможности открывает генная инженерия? Рассказывают ученые Пермского Политеха
Еще до открытия ДНК человек научился выводить представителей животных и растений, соответствующих его запросам. Сегодня возможности генной инженерии позволяют не только создать улучшенный организм «из ничего», но и изменить гены человека, избавив того от болезней. Как работает генная инженерия, где связь между ГМО, вакциной и овощами, что сделали с яблоком, чтобы оно не темнело, и чем чревато создание сверхчеловека, рассказали ученые ПНИПУ.
Как работает генная инженерия?
Генная инженерия — это раздел молекулярной биологии, посвященный созданию искусственных генетических систем с нужными свойствами. Она представлена совокупностью методов, приемов и технологий, позволяющих улучшать существующие наборы генов, — геномы, и создавать новые.
Все сведения о строении и функционировании организма зашифрованы в молекуле ДНК. Эта информация передается от родителей к потомкам, поэтому ее называют наследственной. Молекулу ДНК можно разделить на функциональные участки — гены, в них зашифрована информация о строении конкретных белков. Их набор в организме определяет весь спектр его признаков — вплоть до цвета глаз и структуры волос у человека.
— Таким образом, появление признака у организма определяется наличием определенных белков, а их присутствие зависит от наличия кодирующих их генов. Чтобы добавить новое свойство организму, нам надо ввести в его ДНК ген, кодирующий нужный белок, и обеспечить условия для его экспрессии —протекания многоступенчатого процесса синтеза белка. Или, наоборот, если необходимо избавиться от какой-либо черты, можно удалить соответствующий ген или снизить уровень его экспрессии, — объясняет Анна Ахова, кандидат биологических наук, доцент кафедры химии и биотехнологии ПНИПУ.
Например, чтобы добавить ген в генетический набор организма, его необходимо выделить из ДНК организма-донора, получить большое количество его копий и поместить в модифицируемый организм. Для этой процедуры подойдет любая клетка, и обычно используется материал, который легче извлечь без повреждений донора, например, из крови человека. Выделенный фрагмент может вводиться в свободной форме или в составе вектора — молекулы ДНК, которая способна встроиться в геном хозяина или самовоспроизводиться в его клетках. В качестве векторов применяют плазмиды (небольшие кольцевые молекулы ДНК), фаги (вирусы бактерий), вирусы. Вирусный вектор могут вводить в кровь и другие ткани, а также через ингаляции, то есть вводить непосредственно в организм.
Генная инженерия открывает большие возможности в сферах фармацевтики и медицины, животноводства и сельского хозяйства. Самые увлекательные примеры тому приведены ниже.
Факт 1. Генная инженерия — новейшее поколение инструментов, которые применяются для изменения наследственной информации
Предшественниками инновационного раздела биологии являются селекция и индуцированный мутагенез. Первое — это длительный процесс отбора особей с генетическими изменениями, возникшими естественным путем. Например, домашнюю лису вывел генетик Дмитрий Беляев в 1950-е годы. Произошло это благодаря скрещиванию самых послушных и неагрессивных представителей серебристо-черной лисы.
Второе — искусственное получение мутаций с помощью химического или радиационного воздействия, однако оно слабо поддается контролю. В отличие от этих методов, генная инженерия позволяет редактировать генетическую информацию быстро и направленно.
Факт 2. Генные инженеры смогут создавать ранее не существовавшие формы жизни
Методы генной инженерии позволяют конструировать новые, ранее не существовавшие гены, собирая их из фрагментов ДНК разных организмов или воспроизводя химически. Сейчас ученые работают с модификацией известных науке существ. Однако в будущем технологии позволят создать искусственный организм с нуля. На данный момент известен лишь один пример искусственного организма – небольшая бактерия с синтезированным ДНК.
Факт 3. С помощью ГМО получают вещества, необходимые для жизнедеятельности и здоровья человека
Как объясняет Анна Ахова, генетически модифицированные организмы (ГМО), то есть организмы, генетическая информация которых изменена искусственно, применяются как объекты для научных исследований, в сельском хозяйстве и для производства целевых веществ. Поэтому чаще всего объектами для генетических манипуляций становятся бактерии (в основном, кишечная палочка), мыши, крысы, сельскохозяйственные растения и животные, промышленно-значимые продуценты (организмы, которые могут создавать органические вещества из неорганических), например дрожжи.
— Генные инженеры способны также воссоздать некоторые природные процессы, например, синтез гормонов человека за пределами его организма. Они извлекают ген производства человеческого инсулина и помещают его в бактерию. Ее переносят в условия (питательную среду), при которых она может беспрепятственно синтезировать гормон. На выходе получается производство по получению инсулина, необходимого для людей, больных сахарным диабетом, — рассказывает Анастасия Зорина, кандидат биологических наук, доцент кафедры химии и биотехнологии ПНИПУ.
Еще один пример — при помощи генно-модифицированной кишечной палочки получают гормон роста соматотропин, который необходим для нормального роста и развития детей, поскольку способствует удлинению костей с момента рождения ребенка и до конца его полового созревания. Схожим образом воссоздают белок интерферон, который справляется с вирусной инфекцией.
Факт 4. Манипуляции с генами взрослого человека помогают в борьбе с наследственными заболеваниями
Методы генной инженерии применяют для лечения генетически обусловленных заболеваний, в том числе опухолей. Если развитие заболевания объясняется дефектом одного гена, то его можно заменить здоровой копией. Для этого либо выделяют клетки из организма пациента, генетически модифицируют их и вводят обратно в организм, либо сразу вводят улучшенную ДНК в организм, как объясняет Анна Ахова.
Так работает препарат для лечения β-талассемии — заболевания, при котором из-за дефектного гена снижается способность вырабатывать гемоглобин. Лекарство представляет собой функциональный ген, упакованный в вирус-«переносчик», который встраивается в ДНК стволовых клеток костного мозга (предшественников клеток крови). Кроме того, некоторые виды опухолей пытаются лечить за счет введения в организм генов, кодирующих супрессоры — белки, сдерживающие развитие злокачественных образований.
Факт 5. Вакцины также являются генно-модифицированными продуктами
Например, известная комбинированная векторная вакцина для профилактики коронавирусной инфекции COVID-19. В качестве переносчика выступает аденовирус, в него встроен фрагмент генетического материала коронавируса, кодирующего особый белок, который вызывает иммунный ответ.
— Уникальным вариантом вакцин являются трансгенные растения (томаты, табак, бананы, морковь, картофель), в ДНК которых введены гены, чьи белковые продукты вызывают иммунный ответ. Сейчас разрабатываются съедобные вакцины для профилактики гепатита В, кори, холеры, — рассказывает Анна Ахова.
Как это работает: вирус вводят в молодое растение. По мере его роста, формируются вирусные белки, но не инфекционная часть вируса. Съедая плод с такими белками, иммунитет человека формирует антитела для борьбы с вирусом. Организм становится защищенным, а люди не заболевают.
Факт 6. Нетемнеющие яблоки, безлактозное молоко и противовредительные посевы существуют в наши дни
Генетическая модификация растений обеспечивает повышение урожайности, приобретение устойчивости к гербецидам и насекомым, улучшению внешнего вида и питательности, повышению сохранности. Например, получены яблоки, которые не коричневеют на срезе. Это явление часто объясняют окислением железа, но на самом деле мякоть темнеет за счет окисления антиоксидантов при участии фермента полифенолоксидазы. Снижение экспрессии гена, кодирующего этот фермент, замедляет проявление окраски. Другой пример — это введение в геном растения (табака, кукурузы, риса, зерновых) генов, способствующих синтезу вещества, отпугивающего насекомых. Растение приобретает способность синтезировать токсин, становится несъедобным для вредителей. При этом для человека оно не опасно.
Геном животных улучшают, чтобы повысить скорость их роста, качество мяса или шерсти, сопротивляемость болезням, изменить состав молока, чтобы снизить количество аллергенов, лактозы. Интересно, что первым генетически модифицированным животным, разрешенным к продаже в качестве продукта питания, стал лосось. За счет введения генов из тихоокеанской чавычи и американской бельдюги лосось растет быстрее и в течение всего года.
Почему с генной инженерией стоит быть осторожным?
По словам кандидата биологических наук, доцента кафедры химии и биотехнологии ПНИПУ Анастасии Зориной, в результате халатности ученого, работающего с ГМО, последние могут попасть в окружающую среду, а там начать взаимодействовать с дикими видами. Это способно привести к нежелательным последствиям, в том числе вытеснению дикого видового разнообразия и нарушению экосистем.
— Молекулярно-биологические процессы остаются не до конца изученными, а генетические системы достаточно сложны, поэтому невозможно со 100%-й точностью предсказать все последствия генетических манипуляций. Модификация ДНК может происходить не только в нужных ученым участках, но и в других областях молекулы со сходным строением. При внедрении чужеродной генетической информации может изменяться работа собственных генов. Но это создает трудности лишь для генных инженеров в их попытках получить организмы с заданными свойствами. Не стоит бояться генетически модифицированных организмов и полученных на их основе продуктов, — добавляет Анна Ахова.
— В теории, ученые имеют возможность создать множество модификаций человеческого генома, которые могут дать ему преимущества в борьбе за жизнь: невосприимчивость к вирусам и бактериям, отсутствие наследственных заболеваний, способность к быстрой регенерации клеток и тканей с возможностью отращивать потерянные конечности и т.д. Однако сразу же встает вопрос — имеем ли мы право вмешиваться в законы природы, эволюции? Создание идеального человека может привести, как минимум, к перенаселению. И это только один из множества примеров негативного последствия создания «сверхчеловека», — заключает Анастасия Зорина.
Метастазам мутации не нужны
Злокачественные опухоли расселяются по телу не столько из-за особых метастазных мутаций, сколько из-за ослабления иммунитета.
Злокачественные опухоли возникают благодаря мутациям, из-за которых клетки начинают бесконтрольно делиться. Потом в них появляются другие мутации, обеспечивающие устойчивость к лекарствам. Таких дефектов в ДНК может быть не один, и не два, и не десять: недавно мы писали о том, как исследователи из Медицинского центра Чикагского университета и Геномного института в Пекине насчитали около 100 000 мутаций в опухоли размером 3,5 см в диаметре.
С другой стороны, не все генетические изменения, происходящие в раковых клетках, одинаково важны; некоторые из них ничего не дают опухоли, но зато могут пригодиться потом, когда условия изменятся (например, если одна терапевтическая схема придёт на смену другой).
Одна из самых известных и самых неприятных особенностей рака – это его способность к метастазированию: некоторые злокачественные клетки покидают первичную опухоль и отправляются блуждать по организму, чтобы сформировать где-нибудь вторичный очаг болезни. Поведение метастазных клеток – одна из самых «горячих точек» в современной биологии и медицине, мы едва ли не каждый день узнаём что-то новое, например, о том, как рак выбирает место для вторичной опухоли, как его клетки путешествуют по другим тканям и т. д.
Однако о том, что именно заставляет рак рассылать своих агентов на соседние «территории», до сих пор известно было мало. Логично было бы предположить, что и способность к метастазированию у опухолевых клеток появляется в результате каких-то специальных мутаций.
Жером Галон (Jerome Galon) и его коллеги из института INSERM и других европейских научно-исследовательских центров проанализировали генетическую активность в опухолевых образцах, взятых у 800 пациентов с колоректальным раком. Цель была в том, чтобы найти особые молекулярно-генетические факторы, которые способствовали бы метастатическому распространению злокачественных опухолей.
Среди больных, чьи клетки были взяты для анализа, были как те, у кого рак вёл себя более-менее смирно, так и те, у кого начали появляться вторичные очаги – однако, как пишут авторы работы в Science Translational Medicine, никаких мутаций, которые можно было бы однозначно связать с метастазной активностью, обнаружить не удалось.
Зато отличия были в активности некоторых генов, в частности, тех, что регулируют синтез белка, эндоцитоз и некоторые другие клеточные и иммунные процессы. (На всякий случай заметим, что изменения в активности генов могут происходить без мутационных поправок в ДНК, а просто под действием молекулярных, биохимических, физиологических механизмов – в конце концов, наши гены безо всяких мутаций умеют по-разному работать утром и вечером, в молодости и в старости, и т. д.)
Также удалось заметить, что в метастатических опухолевых образцах было сравнительно мало иммунных цитотоксических Т-лимфоцитов, чья задача – уничтожать раковые клетки. Таких Т-лимфоцитов также было мало у тех больных, у которых вторичных опухолей ещё не было, но блуждающие злокачественные клетки в крови уже появились. Связь между распространением опухоли и активностью Т-клеток удалось показать в опытах на животных: у мышей с пониженным уровнем иммунных «убийц» рак расселялся по организму быстрее.
В целом вывод можно сделать такой: у опухоли изначально есть молекулярно-генетические инструменты, которые позволяют ей колонизировать новые территории, но до поры до времени она не может себе такого позволить – из-за противораковой иммунной защиты. Однако, как только иммунитет ослабеет, злокачественные клетки отправляются в странствие.
С практической точки зрения это означает, что для предотвращения метастазов нужно не искать новые лекарства, которые работали бы против особых метастазных мутаций (таких особых мутаций, как выясняется, просто нет), а стимулировать иммунную систему, в частности, цитотоксические Т-киллеры. Считается, что иммунотерапия в онкологии в принципе может быть намного эффективнее, нежели другие методы лечения, однако у самих опухолей есть целый ряд трюков, которые позволяет им скрыться от внимания иммунной системы, и задача тех, кто занимается онкологическими проблемами, состоит как раз в том, чтобы помочь иммунитету увидеть внутреннего врага.
Автор: Кирилл Стасевич
Продолжаю держать вкурсе
Стартовал эксперимент, приступаем к получению первичной культуры пульмональных фибробластов. Коллеги из фармдепартамента собираются проверять на них какие-то субстанции, даже не спрашивал, какие.
Начинаем с подготовки. Выводим аппаратуру на режимы:
Мешаем рабочие растворы: среды для культивирования клеток, ростовые сыворотки (baby cow juice на сленге заморских товарисчей), растворы для промывки и всякое. Главное - антибиотиков побольше:
Когда коктейль из нутриентов, факторов роста и антибиотиков готов, берем образец ткани крысиного легкого. Фото забора не будет, не хочу вешать тег "жесть". Скажу только, что научно-этическое законодательство блюдем строго. Вот вам сам образец в пробирке:
Ткань воздухоносная, плавает на поверхности. Через 4 часа первичной деконтаминации от возможных бактерий и грибов образец закидываем в ростовую среду с меньшими концентрациями антимикробных препаратов.
Крупный образец измельчаем ножницами (не смотрите на вид, они стерильные) в труху, чтобы было легче отделить клетки от внеклеточного вещества ткани:
Ножниц никогда не достаточно, поэтому окончательное диспергирование ткани производим с помощью ферментного раствора, который хорошо берет коллаген, но клеточную мембрану пройти не в состоянии. Минут через 15 бОльшая часть клеток будет просто плавать в ростовой среде. Их нужно отцентрифугировать, чтобы помыть от следов фермента, а заодно снова поменять среду на чистую . В результате получаем около 12 миллилитров жижицы, в которой плавают клетки.
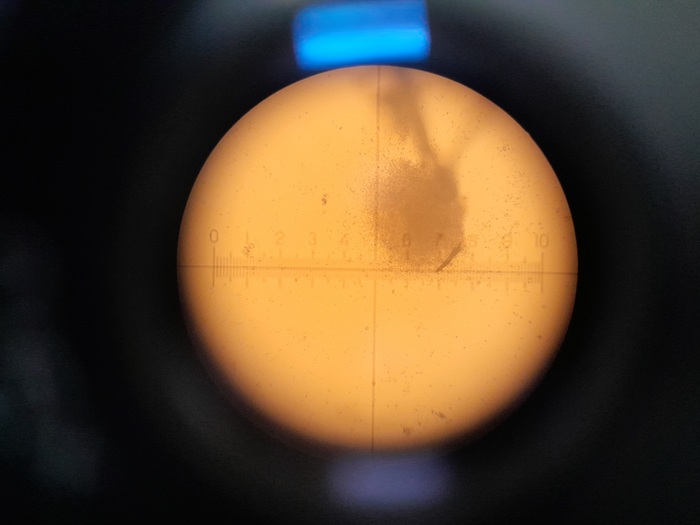
Вот эта пыль - свободно плавающие фибробласты, а крупное скопление, скорее всего, недорастворившийся кусочек ткани легкого.
Остается мелочь - залить клеточную суспензию в специальный флакон, крышка которого имеет встроенный фильтр и проницаема для воздуха. Это нужно, чтобы газовая смесь с аж 5% углекислого газа поступала для дыхания. Так надо, фибробластам так норм.
Последний этап на сегодня - отправить флакон в инкубатор, где он будет стоять в темноте и тепле (37 С), а клеточбки будут делитбся.
Через три дня будет ясно, что там вырастет - благодать или грибной WAAAAGH.
Анимация митоза
Митоз - это непрямое деление клетки, наиболее распространённый способ размножения эукариотических клеток.
РНК лекарства. Синтез нужных белков внедрением матричного РНК
Синтез белка начинается с этапа Транскрипции, когда идёт считывание информации ДНК и построение комплеменнарной ей цепочки матричной или как её называют информационной РНК. Ну а дальше идёт Трансляция- когда рибосома считывает эту информацию с цепочки матричной РНК и преообразует в цепочку аминокислот: пептидов или белков.. . Это вкратце..
Суть идеи внедрения мРНК :
Представим если организм даёт сбои, какие то процессы нарушены, синтез нужного белка идет плохо, или в недостаточном количестве, или же речь идёт в нарушении цепочки ДНК. В этом случае возможно будет внедрять в клетки созданные, нужные цепочки матричного РНК, с которых и будут считывать рибосомы информацию для синтеза нужного белка.
Белковую природу имеют многие структуры организма, ферменты, гормоны, транспортные, структурные, сигнальный... Большинство процессов в организме осуществляются белками. Поэтому нельзя переоценить пользу данного метода.
Скорее это проще чем вырезать и встраивать новые гены в ДНК. Как бы действуя в обход ДНК и стадии Транскрипции.
Возможно таким образом можно будет и усовершенствовать организм, например отправляя в клетку мРНК которая улучшит состояние тканей, придаст им нужную фическую функцию ( прочность, эластичность, устойчивость к каким либо неблагоприятных условиям). Или например применить этот метод для улучшения иммунитета когда это нужно.
Возможно таким образом можно будет омолаживать клетки организма когда, с возрастом, функции синтеза нужныхбелков, каких-либо групп клеток будут нарушены....