«Зомби-клетки» внутри нас
В вашем теле живут клетки-зомби. Они не совсем мёртвые. Такие клетки скорее живые, но они больше не делятся и могут свою «зомби-сущность» передавать соседям. И соседние клетки тоже превращаются в зомби! Зомби-клетки повышают риск рака и разных других заболеваний — например, артеросклероза. Сейчас учёные активно думают о том, как от таких клеток избавиться. Однако есть нюанс: наши внутренние «зомби» выполняют и полезные функции.
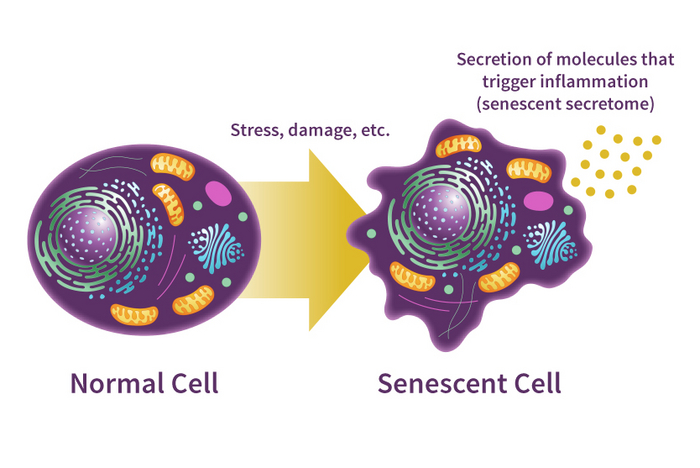
Учёные называют «зомби» сенесцентными клетками. И накопление этого типа клеток в нашем организме — очень важный элемент человеческого старения. Говоря простым языком, сенесцентные клетки — это клетки, которые ранее обладали способностью делиться, но из-за накопления разных повреждений делиться больше не могут. Обычно количество «зомби» с возрастом увеличивается. Из-за этого появляются разные старческие заболевания, возникает боль в суставах, нарушения когнитивных функций, системные воспаления и так далее.
Откуда в нашем теле берутся сенесцентные клетки? Это точно не старые клетки — некоторые «зомби» образуются ещё на стадии эмбрионального развития. Чаще всего сенесцентные клетки, вызывающие заболевания, появляются из-за ошибок, мутаций в ДНК и иных повреждений. Клетка, в которой накопилось много повреждений, выходит из клеточного цикла и как бы говорит: «Всё, я дальше делиться не буду». А ещё «зомби» сигнализируют о своём состоянии иммунной системе, выбрасывая провоспалительные факторы. На эти факторы «приходит» иммунная система и некоторые сенесцентные клетки утилизирует.
Ещё «зомби» могут образовываться из-за повышенной активности отдельных генов. Например, когда клетка подозревает, что может стать раковой, она превращается в сенесцентную. И это хорошо! А сейчас приведу пример, который всем понятен — родинки. Наверняка мои читатели слышали про меланому — рак кожи. Родинки — это не меланома, но в родинках клетки начинают очень активно делиться. Затем в них включается механизм сенесценции — и они делиться перестают. И родинка оказывается «зафиксированной» в своём размере и не превращается в раковую опухоль.
Важно сказать, что сенесцентные клетки могут быть очень разными как по происхождению, так и по свойствам. Поэтому некоторые учёные очень скептично относятся к термину «сенесцентные клетки» — ведь не всегда понятно, какие именно клетки имеются в виду. Интуитивно может показаться, что, раз клетка перестала делиться, значит, в ней что-то сломалось. Но на самом деле «зомби» — это клетки, в которых сработал специальный и целенаправленный механизм, который ограничивает клеточное деление. Так задумано — это не случайная поломка. Это, скорее всего, специальная «поломка» ради предотвращения онкологического заболевания.
Когда клетка сильно повреждается и не может эти повреждения исправить, у неё есть две опции. Первая — запрограммированная клеточная смерть, самоубийство клетки или апоптоз. Вторая — превращение в «зомби». Во втором случае клетка выживает, но перестаёт делиться.
Перед тем как выбрать одну из двух опций клетка пытается себя починить. Когда в клетке повреждается ДНК, включается огромное количество механизмов «репарации». Активируются разные белки, которые пытаются это дело исправить. Однако, если ошибку устранить не получается, клетке приходится выбирать одну из двух упомянутых опций.
Существует по меньшей мере четыре вида сенесценции:
Репликативное старение. У большинства клеток есть встроенный ограничитель делений — предел Хейфлика. При каждом делении кончики хромосом — теломеры — укорачиваются. И через 40-60 делений клетка перестаёт делиться — это и есть репликативное старение. Это старение особенно распространено у крупных видов животных — в частности, у человека;
Сенестенция, вызванная стрессом. Здесь речь идёт не о депрессии, а о том, что клетка может повреждаться из-за ультрафиолетового излучения, ионизирующей радиации, активных форм кислорода и так далее. В результате клетка перестаёт делиться;
Сенесценция, вызванная онкогенами. Онкогены — это гены, чья повышенная активность увеличивает риск рака. Если клетка «замечает» онкогены, то перестаёт делиться;
Сенесценция эмбрионального развития. У человека есть разные эмбриональные структуры, которые не должны чересчур разрастись в утробе. А некоторые структуры даже должны исчезнуть совсем — например, плавники и хвостик у зародыша. Благодаря сенесцентному механизму младенцы появляются на свет без хвоста!
В общем, сенесценция — это довольно нужно и важно. И всё же есть учёные, которые называют сенесцентные клетки «зомби» и считают, что от некоторых из них нужно избавляться — чтобы победить старение.
Итак, у сенесценции есть плюсы и минусы. Сначала расскажу о плюсах. Благодаря «зомби» организм предотвращает появление некоторых онкологических заболеваний. Учёные создавали ГМ-животных с отключенным геном p16. p16 — один из ключевых генов, запускающих сенесцентность. В результате подопытные массово страдали от рака. То есть полностью сенесценцию отключать нельзя! Кроме того, учёные выяснили, что «зомби» иногда помогают регенерировать ткани кожи и мышц. А сенесценция клеток поджелудочной железы может увеличивать выработку инсулина. Сенесценция же клеток печени предотвращает цирроз. В общем, «зомби» делают массу всего полезного. Кстати, такие «зомби» встречаются даже у сверхдолгожителей — голых землекопов.
При этом сенесцентные клетки обладают и рядом «недостатков». Так, с возрастом в нашем теле накапливается очень много «зомби». Особенно опасны клетки, ставшие «зомби» из-за повреждений в ДНК. Они начинают производить молекулы, которые могут вызывать хронические воспаления в тканях вокруг. Так, есть очень важная провоспалительная молекула — интерлейкин-6. Она нужна для коммуникации клеток между собой. Интерлейкин-6 активирует высокую температуру при заболеваниях, влияет на исход некоторых видов рака... Когда клетки перестают делиться из-за сенесценции, порой они начинают производить в 40 раз больше интерлейкина-6. От этого могут повреждаться соседние клетки — и у них тоже включается сенесценция. Происходит цепная реакция.
И ещё один момент: в нашем теле есть «спящие» эндогенные вирусы, которые изначально встроены в наш геном. Они попали туда в ходе эволюции и зашифрованы прямо в нашей ДНК. Так вот, в норме особые клеточные механизмы подавляют вирусы и не дают им сделать ничего плохого. Однако, как показало недавнее исследование, «зомби» не подавляют такие эндогенные вирусы. И в итоге клетка собирает из своего же генома вирусные частицы и заражает ими здоровые клетки. Заражённые клетки, в свою очередь, тоже становятся сенесцентными. Но всё не так плохо: авторы упомянутого исследования создали антитела против вирусных частиц — и остановили заражение.
Но всё же сенесцентные клетки опасны в первую очередь из-за хронического воспаления, которое они вызывают. Инфекции в организме нет, а воспаление есть. И иммунитет борется, по сути, с самим организмом. В итоге из-за хронического системного воспаления возникают артрит, атеросклероз и прочие неприятные «старческие» заболевания. Иногда из-за воспаления возникает рак, деменция, болезнь почек, депрессия. А ещё выраженность системного хронического воспаления очень неплохо предсказывает вероятности смерти человека.
Откуда мы знаем, что сенесцентные клетки существуют и работают? Надо признать: есть учёные, которые скептически относятся к концепции сенесцентных клеток. Как минимум потому, что «зомби» трудно дать точное определение — уж очень разными они бывают. Но одна команда исследователей провела эксперимент, показавший «работоспособность» сенесцентных клеток. Итак, учёные взяли клетки эпителия в предраковом состоянии — в них уже «назрели» мутации, вызывающие рак. Потом эти предраковые клетки исследователи смешали либо с сенесцентными клетками, либо с обычными, несенесцентными, которые могут делиться. А дальше ввели и первую, и вторую смесь подопытным грызунам. Оказалось, что при введении смеси из предраковых и сенесцентных клеток повышается и риск появления рака, и скорость роста опухоли. А при введении другой смеси — с нормальными клетками — таких страшных последствий не наблюдалось.
Считается, что рак — это результат мутаций в клетках. Но на самом деле на успешность и активность раковой клетки влияют ещё и соседние клетки. И если рядом с потенциально мутантной раковой клеткой находятся сенесцентные клетки, шанс развития рака повышается.
Другая команда учёных поставила ещё один опыт — взяла свиные клетки и превратила часть из них с помощью радиации в сенесцентные. Затем и нормальные клетки, и «зомби» исследователи перенесли в почки молодых мышей. Выяснилось, что из-за сенесцентных клеток у грызунов начали возникать фиброзы, воспаления и различные повреждения почек. Похожий опыт провела ещё одна группа учёных: они брали из жировой ткани мышек как сенесцентные, так и нормальные клетки, которые способны делиться. Далее специалисты понемногу пересаживали клетки другим грызунам. Выяснилось, что мышки, которым подсаживали «зомби-клетки», начали проявлять признаки старения — они хуже бегали, становились слабее. Чем больше грызун получал сенесцентных клеток, тем дряхлее он становился. В ходе эксперимента учёные выяснили, что 1 сенесцентная клетка на 10 000 нормальных примерно в 5 раз увеличивает риск смерти.
Что же делать — избавляться от «зомби» или нет? Видимо, надо оставить механизм сенесценции в покое — но при этом можно устранять уже получившиеся «зомби» по мере их накопления. Как это сделать? Наши гены должны активироваться в определённых условиях. Поэтому у каждого гена есть регуляторный участок, который «говорит», где именно и в каких условиях ген будет работать (пример такого участка — промотор, который находится перед началом гена и показывает, с какого места его «считывать»). Так мы можем «подсмотреть», какие гены активируются в сенесцентных клетках. В общем, учёные выяснили, что у существенной части сенесцентных клеток их сенесцентность запускалась уже упомянутым геном p16. У p16, как и у любого другого гена, есть промотор — вот его-то и можно «приделать» к другому гену. Тогда при «запуске» p16 параллельно запустится и тот второй ген. А теперь фокус: приклеиваем промотор p16 к гену, который запускает запрограммированную смерть клетки! Тогда в момент, когда клетка по какой-то причине «решит» стать сенесцентной, она тут же себя и убьёт.
А можно пойти ещё более хитрым путём. Например, сделать так, чтобы наш дополнительный ген, к которому мы приклеили промотор от p16, срабатывал бы только при наличии синтетического вещества, которого не бывает в организме человека. То есть, когда мышке или человеку вводят это секретное вещество, все клетки, где активен p16, убьются. Так исчезнут клетки с повреждённой ДНК, которые больше не делятся. Но будет ли такая «зачистка» полезна для здоровья?
Учёные выяснили, что да, «зачистка» скорее полезна. Исследователи в ходе своего эксперимента удаляли сенесцентные клетки у ГМ-мышей — и продолжительность жизни грызунов немного выросла! При этом животные выглядели моложе сверстников и были более активными, любознательными и бодрыми. Это круто — получается, удаление сенесцентных клеток поможет в борьбе со старением.
Но, увы, такая генная терапия должна происходить до рождения — а мы с вами взрослые люди, нас в эмбриональное состояние уже не вернуть. Что же нам делать? Как избавиться от вредных клеток? Хорошие новости: уже разработаны препараты — сенолитики — которые могут уничтожить некоторые типы сенесцентных клеток. По крайней мере, так показали опыты на животных. Так вот, самая известная комбинация сенолитиков — это дазатиниб и кверцетин. Дазатиниб — это вообще лекарство от рака и опухолей. А кверцетин — это природное вещество, которое достаточно часто встречается в продуктах питания. Исследования показали, что кверцетин усиливает действие дазатиниба.
Я уже описывал эксперимент, авторы которого пересаживали мышам сенесцентные клетки из жировой ткани. Так вот, в той работе учёные брали клетки у ГМ-доноров со светящимися клетками. Клетки доноров отличались от клеток реципиентов, их можно было легко увидеть под микроскопом. В ходе опыта реципиентам давали дазатиниб и кверцетин — и выяснилось, что сенолитики устраняли светящихся «зомби», но не устраняли нормальные светящиеся клетки. А ещё учёные поставили дополнительный эксперимент на старых мышах, чей возраст примерно эквивалентентен возрасту 80-летних стариков. Им давали те же дазатиниб и кверцетин. «С момента лечения продолжительность жизни мышей увеличилась на 36%», — резюмировали авторы статьи. Но на самом деле старые мышки просто чуть-чуть дольше протянули.
Другие учёные показали, что дазатиниб и кверцетин замедляют старение лёгких у мышей. А ещё одни исследователи поставили эксперимент на людях — правда, людей было всего 9, то есть выборка оказалась ничтожно мала. Тем не менее, учёные заявили, что сенолитики снизили число «зомби» в тканях. А вот как препараты повлияли на продолжительность жизни, непонятно — люди, в отличие от мышей, слишком долго живут, на них такие эксперименты ставить сложно.
Кроме микса из дазатиниба и кверцетина, существуют и другие сенолитики. Например, популярен экспериментальный препарат навитоклакс — тоже средство против рака. Вы, наверное, спросите: как противоопухолевое лекарство от рака помогает против сенесцентных клеток? Ведь раковые клетки суперактивно делятся, а «зомби» не делятся вовсе. Но у этих двух типов клеток есть нечто общее — у них постоянно включены «сигналы об ошибке», о повреждениях. Правда, «зомби» в ответ на сигнал перестают делиться, а раковые клетки сигнал игнорируют и очень активно делятся.
В одной работе учёные исследовали сенесцентные клетки в сердцах грызунов. Да-да, в сердце тоже могут появляться «зомби» — это приводит к фиброзу и гипертрофии сердца, что увеличивает риск внезапной смерти. В общем, учёные вызывали инфаркт у мышей. И выяснили, что старые 23-месячные грызуны, которым ранее давали навитоклакс, выздоравливали после инфаркта как 3-месячные мышки. Это как если бы 70-летний старик отошёл от инфаркта как подросток.
К сожалению, у сенолитиков есть побочные эффекты — в частности, малоприятный кашель с кровью. А теперь — к хорошим новостям:
Для борьбы с «зомби» нужны не такие высокие дозировки, как для борьбы с раком;
Сенолитики можно принимать не постоянно, а курсами: попил, а потом дальше живёшь и «копишь» своих «зомби» лет 10-20;
Есть такой сенолитик — квертицин — который идёт в комбо с дазатинибом и почти не имеет побочек. Сам по себе это флавоноид, которого много в разных фруктах и овощах, особенно в каперсах. Правда, есть овощи ради кверцитина бесполезно: чтобы получить нужное количество вещества, придётся есть по полкило каперсов в день. Что делает кверцитин? Он подавляет белок, который не даёт клетке убить себя, говорит ей «Живи!» Грубо говоря, этот белок как психотерапевт. А кверцитин приходит и убивает психотерапевта, а клетка такая: «Всё, не хочу больше жить».
Сейчас много хайпа вокруг ещё одного сенолитика — физетина. Он тоже встречается в разных фруктах и овощах — в яблоках, огурцах, луке, винограде. Биохакеры очень любят кушать физетин! Но есть нюанс. Существует научная программа тестирования интервенций — Interventions Testing Program. Она беспристрастно испытывает всякие средства против старения — три разных лаборатории в США независимо тестируют предлагаемые способы на мышах, самцах и самках. В общем, согласно Interventions Testing Program, физетин жизнь не продлевает.
Но вообще, даже если физетин или другой сенолитик работает на мышах, это не значит, что он будет работать и на нас с вами. Из 100 препаратов, которые работают на грызунах, лишь 10 оказываются эффективными на людях. Так что ждём исследований сенолитиков на людях — чтобы понять, какие из них работают — и работают без серьёзных побочных эффектов.
У нас есть часть тела, где клетки вообще не делятся — это наш мозг. Да-да, нейроны делиться не умеют, а ещё они с годами могут ухудшаться и дряхлеть. У дряхлых нейронов может, например, уменьшаться объём митохондрий. А ещё стареющие нейроны могут выделять интерлейкин-6. А значит, вызывать старческое хроническое воспаление в мозге. То же самое может происходить и с клетками, которые питают и берегут нейроны — например, с астроцитами. И даже у стволовых клеток может случаться сентенция!
В общем, кажется, дела плохи: в нашем мозге, скорее всего, с возрастом настанет старческое хроническое воспаление. Кстати, были опыты, в ходе которых в мозг мышам вводили интерлейкин-6 — и это приводило к ухудшению когнитивных функций грызунов. А ещё учёные знают, что у пациентов с Паркинсоном и Альцгеймером в спинномозговой жидкости находится много противовоспалительных маркёров.
Учёные исследовали влияние сенолитиков на мозг мышей. Оказалось, что сенолитики могут избирательно устранять «сенесцентноподобные» нейроны — повреждённые нейроны, которые вызывают воспаления. И в итоге у грызунов после устранения «проблемных» нейронов улучшились когнитивные способности. Вывод тут простой: лучше потерять немного повреждённых нейронов сегодня, но предотвратить воспаление и сохранить гораздо большее количество здоровых нейронов завтра.
Но всё же пока учёные не знают точно, стоит ли избавляться от «зомби» с помощью лекарств, предназначенных для лечения рака. А ещё устранение сенесцентных клеток — не панацея от старости, ведь «зомби» — лишь один из симптомов этого неприятного процесса. У старения больше дюжины причин!
Тем не менее, обращать внимание на сенесцентные клетки важно, потому что они приводят к системным воспалениям, а такие воспаления — сильный предсказатель смертности у людей. Недаром есть исследование: у людей, которые прожили больше 110 лет, гораздо ниже уровни маркеров воспаления — таких как интерлейкин-6. И это не совпадение. Так что продолжаем изучать сенолитики!
Напоследок расскажу про недавние эксперименты на мушках-дрозофилах. Авторы работы решили объединить два метода продления жизни:
Они удаляли «зомби»;
А ещё омолаживали другие клетки организма с помощью факторов Яманаки, превращая их в стволовые — чтобы они активнее делились и восполняли удалённые дряхлые клетки.
Учёные пришли к выводу, что вместе эти два способа дали результат лучше, чем использование лишь одного метода. Это в очередной раз говорит о том, что старение — это множество разных процессов. И чтобы его победить, нужно использовать одновременно разные методы — чинить митохондрии, увеличивать число стволовых клеток и уменьшать число «зомби», удлинять теломеразу и устранять мутации. Думаю, в будущем возникнет комбинированная терапия против старения — и люди будут жить значительно дольше, чем сейчас.
Крик, Уотсон и Клетка
Корабль медленно двигался вперед, оставляя за собой шлейф на спокойной глади океана, словно путь, проложенный через неизведанные земли знаний. На его борту собрались друзья, коллеги и близкие люди, чтобы проводить в последний путь человека-легенду, чей разум и дух навсегда останутся частью истории.
Уставшее солнце стремилось к закату, прощаясь с миром финальным мазком багряных красок. И, казалось, весь мир склонил голову в знак уважения перед величием ума того, чье наследие обречено на вечность.
« ...Мы собрались здесь, чтобы проститься с человеком, который всю свою жизнь посвятил исследованиям. Он говорил, что истина кроется в простоте и красоте естественного порядка. И сейчас, стоя перед бесконечностью океана и неба, я не могу не вспомнить его слова: «Ты прав, дружище, природа оказалась гораздо лучшим художником, чем люди...».
Прах Фрэнсиса Крика устремился в океан, ветер бережно подхватывал его частицы и уносил по только ему известному пути, сливаясь с водой, воздухом и самой сутью жизни на Земле.
***
Некто — крайне умные и глубоко эрудированные — подтверждают:
1943 год, Чикаго. Пятнадцатилетнему Джеймсу Уотсону удается получить стипендию для одарённых юношей. Он погружается в академический мир, где наука жаждет открытий. Вооружённый неутолимым упорством познания тайны странной молекулы, он отправляется в путешествие по миру науки.
В то время, когда многие учёные ещё не осознавали или не признавали значение ДНК для наследственности, серия значимых исследований уже начала постепенно раскрывать её тайны.
Фредерик Гриффит, будучи одним из пионеров в 1928 году, показал, как наследственная информация может передаваться от одного организма к другому. Он выявил способность бактерий «передавать» свои генетические характеристики другим бактериям, назвав это явление «трансформирующим принципом».
Эта идея, переданная следующему поколению учёных, предвосхитила открытие Освальда Эйвери, который позже доказал, что именно ДНК, а не белки, является носителем этой информации. Эти открытия стали фундаментом для дальнейших исследований Джеймса Ватсона, уже защитившего к тому времени докторскую диссертацию в Индианском университете.
Уотсон, полный идей и вдохновения, отправляется в Кембридж, где его ожидает судьбоносная встреча с Фрэнсисом Криком — острым на слово шутником и любителем провокационных споров. Несмотря на различия в характерах и подходах, они быстро находят общий язык в стремлении раскрыть тайну ДНК.
К моменту их встречи в 1951 году, Фрэнсис Крик уже известен в научном мире. Он работает над теорией, как информация передаётся внутри клеток. Согласно его правилу, всё начинается с ДНК, переходит в РНК (копия ДНК), а затем превращается в белки — строительные блоки нашего тела. Эта «центральная догма» подчёркивала его уверенность в процессе, предвосхищая даже обратный перенос информации от РНК к ДНК, открытый уже после ухода Крика.
И вот, наконец, момент великого триумфа: 1953 год становится знаковым благодаря нечаянному открытию, сделанному Фридрихом Мишером в далёком 1869 году. Он обнаружил нечто, что не было ни белком, ни углеводом, и назвал это вещество «нуклеином». Мишер даже представить себе не мог, насколько велико его открытие и как далеко оно его продвинет в истории науки.
Это открытие не просто подтвердило предшествующие исследования, но и открыло дверь в новую эру молекулярной биологии, генетики и биомедицины.
Но обо всем по порядку. Вы когда-нибудь задумывались, как долго живёт отдельная клетка в вашем организме? Или, что важнее — рецепт, повар или ингредиенты? Как вы смотрите на перспективу, что части вашего тела могут восстановиться сами, подобно хвосту ящерицы?
Срок жизни клетки варьируется в зависимости от её типа и роли в организме. Например, кожные клетки живут около 2-3 недель, а клетки печени обновляются каждые 300-500 дней. Нейроны, или нервные клетки, живут всю жизнь своего хозяина, не обновляясь.
Представьте себе клетку как обычную кухню, где мы проводим значительную часть времени. В каждой клетке-кухне есть Инструкция — ДНК, диктующая, как выглядеть, функционировать и как болеть. По другому, ДНК — это кулинарная книга для создания различных частей человеческого тела. Когда клетке нужно что-то сделать (например, построить новый волосок или залечить царапину), она копирует нужный рецепт из книги ДНК и переносит в РНК (копия ДНК), которую можно считать скороваркой, готовящей блюдо — Белок. Сформированные в результате процедурного копирования клетки по рецептам ДНК белки являются строительными блоками тела, нужными для роста, движения и защиты от болезней.
Вот как это устроено:
1. ДНК составляют две длинные цепи, которые скручиваются в двойную спираль вокруг одной оси;
2. Молекулы в этих цепочках соединяются парами: аденин (A) с тимином (T) и цитозин (C) с гуанином (G);
3. Благодаря структуре двойной спирали ДНК может копировать себя перед каждым делением клетки, что обеспечивает точное дублирование информации;
ДНК в клетке — это инструкция, указывающая, как «ремонтировать» и поддерживать все части нашего тела. Всё это тесно связано и эффективно работает вместе, чтобы мы были здоровы и умны!
Рождение структуры ДНК аккуратно перелистнуло страницу в науке, предоставив человечеству бесчисленные возможности.
В 1962 году, потрясенный открытием мир наградил Джеймса Уотсона и Фрэнсиса Крика Нобелевской премией по физиологии и медицине, отправив их имена в вековую вечность. Вместе с ними в ту же вечность отправились Морис Уилкинс и Розалинд Франклин, чьи рентгеноструктурные исследования ДНК проложили дорогу к пониманию её двойной спирали. Именно фотографии, созданные в лаборатории Уилкинса и, особенно, Франклин, стали ключевым доказательством теории, предложенной Уотсоном и Криком. Однако, в то время как Уилкинс встал на третью ступень пьедестала славы, Розалинд Франклин была оставлена за кулисами, несмотря на её безупречный вклад.
Ужасная несправедливость, но правила Нобелевской премии не позволяют награждать ушедших в мир иной. Во времена, когда мало что было известно о рисках радиации, Розалинд часто подвергалась её воздействию, особенно, когда занималась исследованиями ДНК. Многие считают, что именно это привело к её заболеванию раком яичников. 16 апреля 1958 года, в возрасте 37 лет, она умерла, оставив после себя наследие, которое трудно переоценить.
Получение Нобелевской премии стало только началом сложного жизненного пути Джеймса Уотсона. В 1968 году он взялся за научную и административную работу, возглавив Лабораторию Колд-Спринг-Харбор. Джеймс Уотсон стал ключевой фигурой в проекте "Геном человека", открыв новые горизонты для человечества. Он также опубликовал ряд книг, включая "Двойную спираль", где рассказал собственную историю одного из величайших открытий двадцатого века.
Фрэнсис Крик после работы над ДНК переключил свой научный интерес на изучение мозга и сознания. В 1976 году он переехал в Салк Институт биологических исследований в Сан-Диего, Калифорния, где работал над проблемами нейронауки. Крик изучал, как мозг воспринимает зрительную информацию и как формируется сознание. Он считается одним из пионеров в области нейробиологии сознания. Френсис Крик продолжал активно работать и публиковать научные статьи вплоть до последнего дня. После смерти в 2004 году, в соответствии с завещанием Фрэнсиса Крика, его тело было кремировано, а прах рассыпан в море.
Привет, человеки и человекини!
Пусть каждый прожитый день приносит вам маленькие, но невероятные открытия. Наш мозг не знает границ, как любят повторять крайне умные и глубоко эрудированные. Поэтому, позволяйте собственным мыслям хоть ненадолго вырваться за пределы повседневных ограничений.
Если бы вы могли добавить в свою ДНК одну характеристику любого животного, что бы это было?
А) Способность восстанавливать потерянные или поврежденные части тела;
Б) Возможность видеть в темноте;
В) Способность прыгать на 6-8 м и развивать скорость до 80 км/ч.