Гордился сын способностью отца
Крушить плазмодий неустанно, без конца.
Он по стопам его пошел и обогнал,
"Я из семьи бигуанида!" - потомок это твёрдо знал.
Для патогена он непобедим.
Теперь отец гордится им.
Нужных ионов вам, уважаемые подписчики сообщества и товарищи читатели! Аспирин из предыдущего поста, конечно, это дело известное, ведь многие хоть раз в жизни им пользовались. Этот анальгетик не подводит людей многие годы, но в медицине есть далеко не только убийцы боли, но и еще один не менее интересный класс препаратов - дезинфектанты, антисептики. Между прочим, эта группа веществ подарила мне некогда массу приятных впечатлений, позволив мне лицезреть немало любопытных явлений. Зачем я снова пришёл сюда? Скоро узнаете.
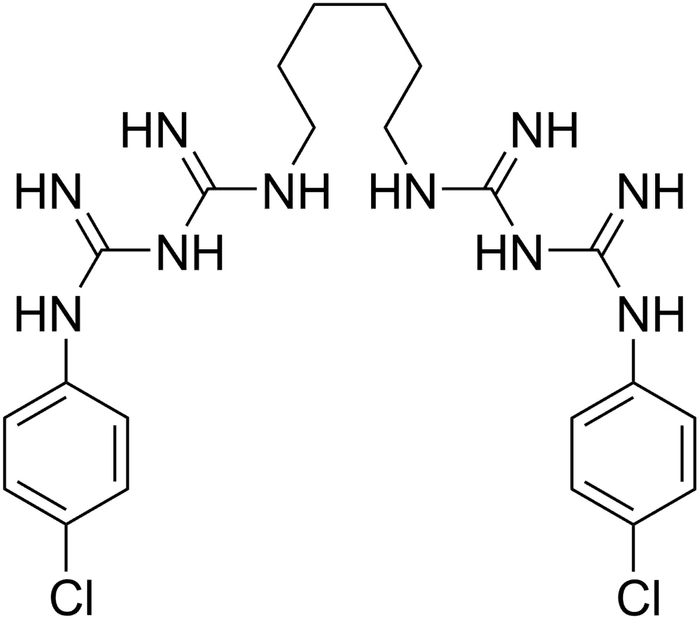
Громоздкая молекула, не так ли? Это она здесь еще по-художественному представлена, чтобы ваш перфекционист смог насладиться симметрией нашего гостя.
Этот препарат даже и гостем-то не назовешь, ведь он почти все время с нами, поэтому будем величать его скорее "знакомым". Итак, наш старый знакомый на страже нашей безопасности вот уже более 60 лет! Дело всей его жизни - охрана чистоты и относительной стерильности покровов тела человека, если можно так выразиться. В быту люди доверяют его растворам с содержанием активного вещества всего в 0.05%. Разумеется, есть разновидности и пожестче (0.5%), но в быту они менее популярны. Почему не производят еще более ядреных составов, для меня пока загадка. И это при том, что хирурги иногда дезинфицируют руки аж 20% р-ром! Хотя надо полагать, что аптечная форма более универсальна и подходит для широкого диапазона применений - от обработки ран до полоскания горла. Как бы там то ни было, ЛВ (лекарственное вещество) довольно эффективно в своей сфере, раз даже столь сильное разведение ни мешает веществу вершить свои благие дела. По своей известности среди доступных антисептиков оно уступает разве что перекиси водорода, а найти его я смог даже за пределами аптеки, ведь некоторые фирмы добавляют ЛВ в состав своих комплексных дезинфектантов, а некоторые просто выставляют его на полки обычных супермаркетов (в моем регионе есть такие точки). В химическом отношении является дихлорсодержащим производным бигуанида(его отец, что занимался истреблением малярийных плазмодиев). По структуре весьма близок к бигумалю. Механизм действия хлоргексидина заключается во взаимодействии с фосфатными группами на поверхности клетки, вследствие чего возникает смещение осмотического равновесия, нарушение целостности клетки и её гибель. Наводит страх, в основном, на грамотрицательных и грамположительных бактерий, а также их дружков вроде некоторых вирусов и внутрибольничных инфекций.
Утомились уже ждать, когда я назову его имя? А вот он, перед вами: хлоргексидина биглюконат.
Все проводимые мной реакции просты и их легко воспроизвести даже обывателю, никогда не державшему в руках пробирку. Перечень для тех, кто хочет сразу приступить к тестам:
Р-р хлоргексидина биглюконата 0.05% - аптека
Р-р сульфата железа (III) - окисляете р-р железного купороса из садоводческого магазина обычной перекисью до насыщенного ржавого окраса и готово
Р-р сульфата меди - строймагазины/садоводческие магазины
Спиртовка или другой источник огня (да хоть свеча)
Р-р иода спиртовой 5% - аптека.
Серная разб. кислота - сернокислый электролит для аккумуляторов
Можно начинать!
Если сидеть и разглядывать формулу и структуру хлоргексидина, то на ум навряд ли сразу придет что-то толковое. Учитывая, что реактивов у нас нескромно мало, будем опираться на самое доступные и достоверные источники. Таковыми я обычно нахожу фармакопеи, которые частенько подсказывают мне многие испытания на подлинность. И на этот раз поступим так же. Среди тамошних реакции в первых строках видим описание испытания с сульфатом меди. Как правило, все инструкции в фармакопеях пишутся строгим официальным наречием, исключающим любое ваше возражение в случае неудачи. Да-да, не всегда описанное в фармакопеях можно с точностью повторить, но мы все же попытаемся. Почему же я все-таки сомневался?
В качестве первого взаимодействия предлагается познакомить препарат с сульфатом меди. Однако вследствие сильного разведения ЛВ в растворе нужно брать всего несколько капель купороса, иначе эффект реакции заметно ослабевает. Повторяем первый шаг и наблюдаем такую картину: р-р препарата хоть и ожидаемо окрашивается в голубой, но вскоре наш глаз замечает, что он не просто голубой, но еще и мутный. Действительно, сульфат меди провоцирует помутнение р-ра, но природу явления пока объяснить не удается.
Смело ставим р-р над огнем и ждем чего-нибудь интересного. Но реакция так просто не хочет себя обнаруживать, поэтому вы можете довести р-р до кипения, но может ничего не произойти. Но если внимательно присматриваться, то концу взаимодействия вы увидите странные частицы у поверхности р-ра. Дайте смеси чутка остыть, и сможете увидеть искомое соединение. Оно представляет собой сиреневые хлопья, обычно локализующиеся сверху. Их всегда образуется очень немного, так что отфильтровать, высушить и досконально изучить пока не представляется возможным. Однако именно так выглядит первая реакция, доказывающая подлинность хлоргексидина.
О природе неизвестного вещества у меня до сих пор ходят слухи, на сей момент я предположил, что соединение имеет отдаленное сродство с биуретами. Вспомните школьную качественную реакцию на белки: к пробе подливают сульфат меди и щелочь, что в итоге заставляет белок засиять красивым фиолетовым отливом. Эту реакцию кличут биуретовой реакцией. В нашем случае имеется углеродная цепь, сплошь утыканная вторичными аминогруппами. Есть гипотеза, что эти самые аминогруппы "обхватывают" ионы меди, образуя те самым медьсодержащие комплексы, наподобие хелатных. В обыкновении, такие хитро устроенные молекулярные здоровяки являются окрашенными. Аминогрупп у хлоргексидина предостаточно, так почему и нет? Таковы догадки.
Видео нет, т.к. на камеру адекватно заснять образование комочков не получается, только на фото ловятся
Да, такая вот "сирень". Немного, но все же есть. А вы чего ждали? :)
Если принять эту гипотезу, то непонятным остается одно: почему для реакции нужно именно нагревание? Понятно, что накал страстей повышает реакционноспособность, но что конкретно мешает проводить такие взаимодействия без него? Лады, идем дальше.
Второй реакцией нам советуют бахнуть щедро сульфатом железа 3+. Условия проверки те же: влить несколько миллилитров и нагреть. Беспрекословно подчиняемся строгим инструкциям и вот что мы получаем.
И вновь сначала ничего особенного, опять р-р слегка мутнеет, а в толще его распространяется желтизна сульфата. Повысим, так сказать, градус! Заносим пробирку в самое жар-пекло.
Видео ускорено в 8 раз
На сей раз заснять все было просто, после баньки светло-желтый р-р помрачнел и стал как будто более ядреным, а цвет его сменился на бурый. При попытке описать итоги опыта пред нами встал следующий вопрос: а не появился ли этот окрас в результате образования золя гидроксида железа (III)? Если вы когда-то изучали основы физической коллоидной химии или, как ее ласково зовут студенты, "физколды", то вы наверняка помните раздел о золях и условиях их существования. Может быть, вы даже проводили опыт с нагреванием на водяной бане р-ра хлорида железа (III), где вы должны были наблюдать аналогичное помутнение. Там молекулы хлорида железа (III) в водном растворе подвергаются частичному или полному гидролизу с гидроксидом на выходе. Не будем вдаваться в подробности и объяснять природу мицелл, но суть вам ясна. Что говорят фармакопеи? По их словам, р-р должен стать чуть красноватым, а точнее, цвет должен стать тёмно-оранжевым. Мы этого фактически добились, а вот в случае с золем этого бы мы не заметили, там окрас мало бы чем отличался от исходного.
Что же мы получили? Полагаю, что механизм реакции не сильно отличен от предыдущей, просто теперь места ионов меди заняли ионы железа.
Третьей реакцией, с которой можно поиграть в фармацевта-следователя станет реакция с р-ром иода, она уже не фармакопейная, а моя. Несмотря на то, что р-р иода с иодидом калия часто применяют как осадительный реактив для идентификации третичного азота, мы будем юзать этот реактив и без наличия такого азота. добавок к этому мы будем еще и подкислять р-р серкой. Просто настойка иода ничего не может сделать, но низкий рН к ней приходит на помощь. Р-р приобретает необычный цвет, когда такое случается в пробах на третичный азот, фармакопеи его зовут "красно-фиолетовым". Честно скажу: представить такой оттенок мне не под силу. Сразу видно: сколько глаз - столько и фраз, каждый из наблюдателей усмотрел что-то свое.
Одно ясно точно: в кислой среде с настойкой иода р-р приобретает загадочный "красно-фиолетовый цвет". И это опять какая-то муть
После всех предыдущих реакций возникло странное ощущение, что здесь что-то не так. Все р-ры в той или иной степени мутнели, а при проверке выяснилось, что все добавленные к ним ранее соли имели кислую среду при гидролизе. С иодом в той же кислоте случилось нечто похожее. Значит, надо обратить внимание на низкий рН. Добавим-ка просто серки:
Помутнел. Что и требовалось (?) увидеть
Хлоргексидин биглюконат не любит кислую среду. Возможно, деградации при этом не происходит, но что тогда мы видим? Это мне пока разгадать не удалось. Есть даже гипотеза, что виновником всех реакций является не сам хлоргексидин, а именно те самые две молекулы глюконовой кислоты. Не упускайте из виду существование глюконатов! Можно было бы сказать, что серная кислота выталкивает глюконовую, но выталкивать ее просто некуда, ибо последняя растворима в воде. Да и с медью получился бы не сиреневый осадок, а красный оксида меди (I), т.к. восстановление. Обратиться к фармакопеям не вариант - они молчат и ничего более не скажут. Поэтому практика - это наши глаза и наши руки. Теория вам такого никто не покажет. И еще большой вопрос, кто там правее.