Иммунная система человека очень хорошо справляется с львиной доли задач, который на неё возложены. Тем не менее время от времени какому-нибудь паразиту удается проскользнуть сквозь эту сеть и устроиться внутри. Своим успехом это существо обязано не просто какому-то недосмотру или ошибке, а собственному умению обойти и обмануть иммунную систему. У бактерий и вирусов имеются свои уловки, но большую часть самых интересных стратегий можно обнаружить у «классических» паразитов — простейших, трематод, ленточных червей и других эукариот. Они умеют уклоняться от встречи с иммунной системой, отвлекать ее, изматывать и даже брать под свой контроль, ослабляя или при необходимости усиливая подаваемые ею сигналы. Признаком изощренности их методов может служить тот факт, что вакцин против подобных паразитов не существует, тогда как вакцины против бактерий и вирусов давно стали привычным явлением.
Посмотрим, как же им это удается.
Сонная болезнь.
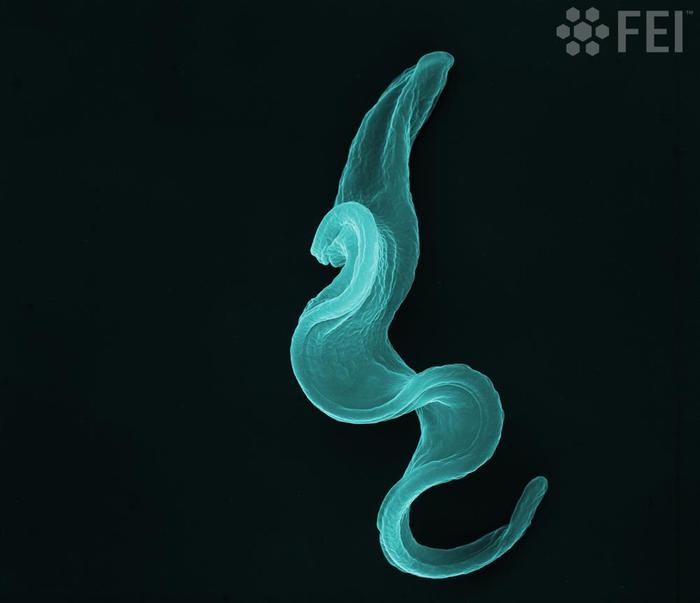
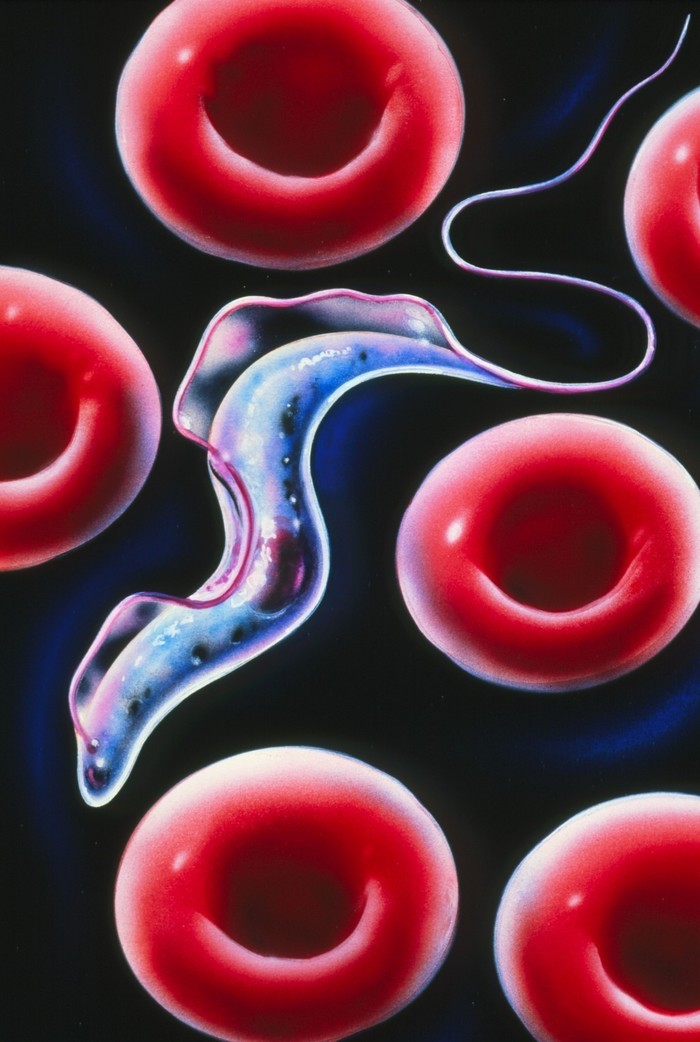
Ее причиной является простейшее Трипаносома, переносимое мухой Цеце.
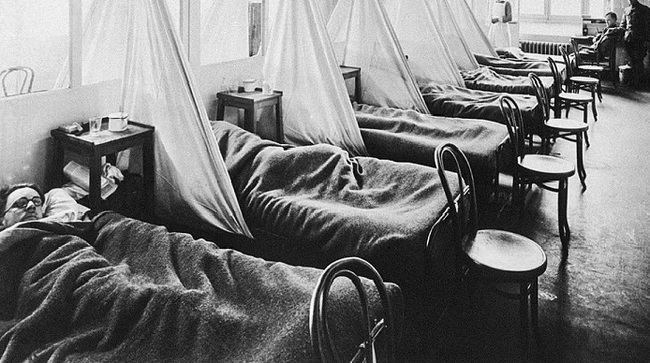
Болезнь эта, как вы наверняка знаете, очень страшная. Весьма беспечные африканцы, плюющие на СПИД, во многих районах Африки не рискуют заниматься разведением скота из страха перед мухой Цеце и сонной болезнью.
Ее симптомы - лихорадка и зуд, а впоследствии - опухание лимфатических узлов, спутанное сознание, сонливость, плохая координация движений, онемение и почти гарантированная смерть при отсутствии лечения. А лечение производится лекарством, на 20% состоящим из мышьяка и вызывающим жуткие побочные эффекты. Вдобавок, его часто приходится прерывать в связи с тем, что лекарство ведёт пациента к могиле быстрее самой болезни. В ее разгар кровь больного буквально кишит трипаносомами — в каждой капле можно было насчитать тысячи существ, но в крови умершего пациента их может не обнаружиться вообще.
Сегодня, после более ста лет исследований, ученые по-прежнему не в состоянии изготовить вакцину от сонной болезни, но теперь они по крайней мере понимают, кактрипаносомы умудряются противостоять иммунитету хозяина до самой его смерти. Оказалось, эти существа играют в очень утомительную игру, которую можно было бы назвать «заманить и подменить».
Если бы вы смогли увидеть поверхность трипаносомы в мельчайших подробностях, зрелище, вероятно, показалось бы вам скучным. Больше всего оно напоминало бы однообразнейшее кукурузное поле: миллионы стеблей, стоящих сплошным ковром почти без промежутков между ними.
Посмотрите на соседнюю трипаносому, и не увидите ничего нового: «стебли» точно так же торчат из ее шкуры густой щетиной. Если рассматривать любую из миллионов и миллионов трипаносом, обитающих в любой момент болезни в теле человека-хозяина, вы, скорее всего, увидите ту же картину.
Для иммунной системы человека эти паразиты должны быть легкой жертвой — примерно как рыба в бочке. Стоит иммунной системе познакомиться всего с одной из этих бесчисленных молекул-стеблей и запомнить ее, и она сможет истребить практически всех паразитов в организме. И в самом деле, когда В-клетки хозяина начинают производить антитела, настроенные на молекулы-стебли, трипаносомы начинают умирать. Но не вымирают полностью. В тот момент, когда кажется, что все трипаносомы в теле вот-вот исчезнут навсегда, их численность достигает минимума и вновь начинает расти. Их вид меняется, и если вы теперь будете пролетать над трипаносомой, то увидите не кукурузное поле, а пшеничное —тоже однообразный до предела пейзаж, но совсем другой.
Причина такой быстрой и резкой перемены — в уникальной организации генов трипаносомы. Все инструкции по строительству молекулы, которая служит строительным материалом для оболочки паразита, расположены в одном- единственном гене. Обычно при делении трипаносомы у новых особей под действием этого гена возникает точно такая же поверхность. Но примерно один раз за десять тысяч делений трипаносома вдруг отправляет этот ген в отставку — вырезает его с законного места в собственной ДНК. Затем паразит обращается к резервному запасу из тысячи с чем-то других генов, отвечающих за строение поверхности, выбирает из них один и вставляет его в ДНК на место прежнего. И поверхностную молекулу трипаносомы начинает формировать новый ген: эта молекула похожа на предыдущую, но не идентична ей. Теперь иммунной системе, успевшей сосредоточиться на предыдущем облике чужака, требуется время на перенастройку— на то, чтобы опознать изменившегося паразита и изготовить для него новые антитела. Пока этого не произойдет, трипаносомы с новым обликом будут в безопасности и смогут стремительно размножаться. Когда же иммунная система перенастроится и начнет охоту за трипаносомой с новым антителом, где-нибудь успеет объявиться паразит с третьей разновидностью гена и, соответственно, третьим видом оболочки. Гонка может продолжаться несколько месяцев или даже лет — за это время трипаносомы успевают сбросить и поменять шкурку сотни раз. В крови хозяина накапливается множество самых разных фрагментов трипаносом, его иммунная система приходит в состояние перманентного перевозбуждения и атакует клетки собственного тела. В конце концов жертва умирает.
Такая стратегия работает только потому, что у паразита имеется запас готовых генов, каждый из которых может отвечать за строительство молекул поверхностного слоя. Но эти гены невозможно извлекать из «загона» в произвольном порядке. Трипаносомы перебирают свой запас генов в строго определенном порядке, по очереди. Возьмите две идентичные трипаносомы и заразите ими двух мышей, и их потомки будут менять гены и оболочки в одинаковом порядке. Таким образом паразит может растянуть свое существование в организме хозяина на многие месяцы, а там, глядишь - и новый хозяин найдется.
Похожую страгегию применяют и плазмодии, вызывающие малярию Паразиты. Часть 4. Малярия .
Но если трипаносома сразу вступает в борьбу с иммунной системой, то плазмодий сначала от нее бегает.
Попав впервые в тело через укус комара, он способен за полчаса добраться до печени; за это время иммунная система часто не успевает заметить чужака. Оказавшись в печени, плазмодий прячется в одну из клеток, где созревает и одновременно привлекает к себе внимание организма. Инфицированная клетка печени хватает случайные протеины плазмодия, свободно плавающие внутри, разрезает их на части и отправляет наверх, чтобы выставить для всеобщего обозрения на своих молекулах МНС. Иммунная система хозяина распознает эти антигены и начинает готовить атаку на больные клетки печени. Но подготовка требует времени — достаточного, чтобы паразит успел разделиться на сорок тысяч копий (это займет примерно неделю), вырваться из печени и приняться за клетки крови.
К моменту, когда иммунная система будет готова уничтожить зараженные клетки печени, от клеток останутся одни пустые оболочки.
Тем временем паразиты заселяются в эритроциты и обустраивают свой новый дом. Плазмодию приходится приложить массу усилий, чтобы компенсировать отсутствие у клеток крови генов и протеинов, но у пустоты есть и положительные моменты: в красных кровяных клетках очень удобно прятаться. Поскольку в них нет генов, они не умеют строить и молекулы МНС, а значит, никак не могут сообщить иммунной системе о том, что появилось у них внутри. Некоторое время плазмодий, проживая внутри эритроцита и пользуясь его идеальной маскировкой, может наслаждаться полной безопасностью. Но паразит активно делится, быстро заполняет клетку и в какой-то момент начинает укреплять стенки эритроцита собственными протеинами. Чтобы не погибнуть вместе с эритроцитом в селезенке, он строит на поверхности клетки специальные выросты и снабжает их крохотными защелками, способными зацепиться за стенку кровеносного сосуда и накрепко приковать к ней клетку-дом.
Эти защелки представляют собой отдельную опасность: они рискуют привлечь к себе внимание иммунной системы. Против них могут быть изготовлены антитела, и тогда соберется целая армия Т-киллеров, которые смогут легко узнавать по этим признакам инфицированные клетки.
Поскольку иммунная система способна опознавать эти защелки, ученые потратили немало времени на их изучение в надежде разработать вакцину против малярии. В 1990-х гг. они впервые смогли установить последовательность генов, отвечающих за создание защелок. Выяснилось, что для их строительства достаточно лишь одного гена, но в структуре ДНК плазмодия таких генов больше сотни. Получается, что защелки бывают самой разной формы, но каждая из них способна прочно прикрепить эритроцит к стенке кровеносного сосуда.
Впервые забравшись внутрь эритроцита, Plasmodium включает одновременно множество генов, отвечающих за строительство захватов, но выбирает для оболочки своего дома защелок лишь одного типа. Таким образом, поверхность эритроцита покрывается защелками одинаковой формы. Наконец клетка разрывается, и из нее выходит шестнадцать новых паразитов. В следующий раз каждый из них почти наверняка воспользуется тем же геном и снабдит свой новый дом-эритроцит защелками той же формы, но время от времени один из паразитов переключается на другой ген и делает защелки на своем эритроците неузнаваемыми для иммунной системы. Да, именно так: плазмодий умудряется спрятаться на самом виду; к моменту, когда иммунная система научится узнавать новые защелки, паразит перейдет на следующую модель. Иными словами, возбудитель малярии пользуется точно такой же стратегией «заманить и подменить», что и возбудитель сонной болезни.
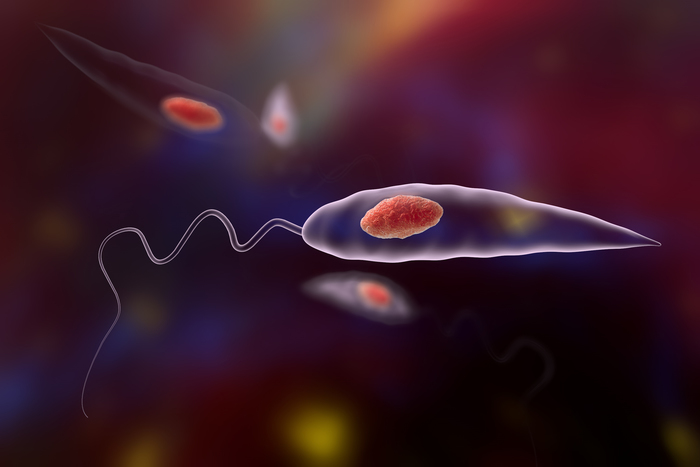
Плазмодий — лишь один из множества паразитов, которые живут внутри наших клеток. Одни из них способны жить в любых клетках, тогда как другие выбирают клетки только одного типа. Есть такие, которые специализируются на самых опасных клетках, макрофагах, чья работа — убивать и пожирать паразитов. К последней категории относятся и простейшие Leishmania.
Любой из более чем десятка видов этого паразита переносится от человека к человеку через укусы насекомого, известного как москит, или песчаная мошка. Каждый вид этих простейших вызывает собственную болезнь. Leishmania major вызывает кожный лейшманиоз — неприятный волдырь, который затем превращается в язву. Leishmania donovani нападает внутри организма на макрофагов и меньше чем за год может убить хозяина. Leishmania brasiliensis, третий паразит рода Leishmania} вызывает эспундию — злокачественный лейшманиоз, при котором паразит вгрызается в мягкие ткани головы до тех пор, пока его жертва не лишится лица.
Лейшмании не приходится проникать в макрофаги хозяина силой, как плазмодий проникает в эритроциты. Лейшмания больше напоминает вражеского лазутчика, который стучит в двери полицейского участка и просит, чтобы его арестовали.
Попав в организм человека с укусом москита, этот паразит привлекает к себе молекулы комплемента; те пытаются просверлить его мембрану и в свою очередь привлекают макрофагов, которые по идее должны сожрать чужаков. Лейшмания вполне способна пресечь все попытки комплемента нарушить целостность ее оболочки, но сами молекулы она не уничтожает. Напротив, она позволяет комплементу выполнить вторую часть задачи: послужить маячком. Прибывший на место макрофаг проползает по паразиту, обнаруживает комплемент и открывает в своей мембране отверстие, чтобы сожрать лейшманию.
Макрофаг проглатывает паразита, и тот оказывается внутри, в пузырьке. В принципе, этот пузырек мог бы стать для паразита камерой смерти. Макрофаг мог бы слить пузырек-тюрьму с другим пузырьком, наполненным молекулярными скальпелями, и приступить к расчленению лейшмании. Но каким-то образом — ученые до сих пор не знают, каким именно, — лейшмания останавливает слияние пузырьков, и пузырек-тюрьма становится для паразита удобным домом.
Лейшмания не только воздействует на того макрофага, внутри которого находится, но и меняет всю иммунную систему организма. Когда молодые Т-лимфоциты в первый раз встречаются с антигенами и сцепляются с ними, они могут превратиться в Т-хелперы. Хелперами какого типа они станут — воспалительными или теми, что помогают В-клеткам производить антитела,—зависит от соотношения определенных сигнальных признаков, циркулирующих по телу.
Сначала оба типа Т-клеток свободно размножаются, но через некоторое время начинают взаимодействовать друг с другом. При многих инфекциях результат именно этой борьбы склоняет чашу весов в пользу одного из двух типов Т-клеток. После этого победившая сторона ведет войну с паразитами по собственным правилам.
Лейшмания научилась решать исход этой схватки. Очевидно, что лучшим способом уничтожить паразита было бы произвести множество воспалительных Т-лимфоцитов, которые могли бы помочь макрофагам расправиться с проглоченными паразитами.
Именно это, судя по всему, происходит в организмах тех людей, кому удается справиться с лейшманией. Паразитологи провели интересный эксперимент. Заразив мышей лейшманией, они отсасывали воспалительные Т-лимфоциты из крови мышей, перенесших инфекцию, и вводили их мышам, генетически почти лишенным иммунной системы. Эта инъекция позволяла беспомощным мышам столь же успешно справляться с паразитом.
Но очень часто нашим телам не удается наладить надлежащую оборону, и эта неудача играет на руку лейшмании. Сидя внутри хозяина-макрофага, паразит вынуждает его испускать сигналы, которые склоняют чашу весов в пользу Т-лимфоцитов, помогающих В-клеткам производить антитела. Но внутри макрофага лейшмания находится в полной безопасности, антитела никак не могут до нее добраться. Болезнь развивается.
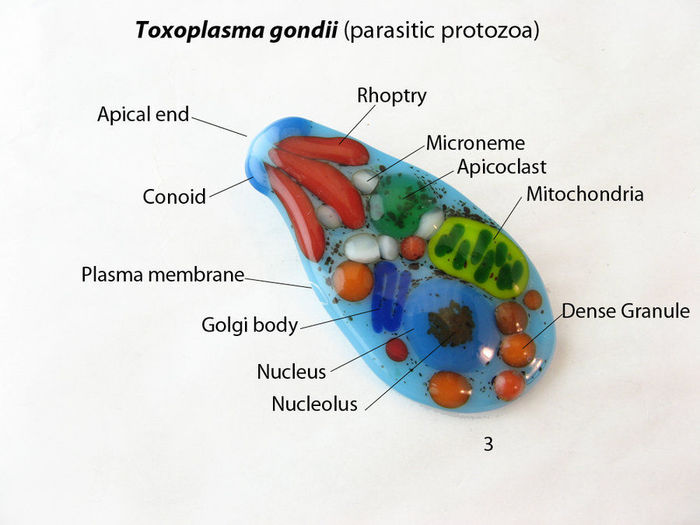
Плазмодий и лейшмания весьма разборчивы при выборе дома: эти паразиты могут жить только в клетках определенного типа. Большинство паразитических простейших не менее привередливы, но некоторые способны неплохо устроиться в клетке практически любого типа. Один из таких видов—Toxoplasma gondii, существо, пребывающее в незаслуженной безвестности.
Мало кто вообще знает о токсоплазме, хотя существует реальная вероятность того, что мозг множества ничего не подозревающих людей несет в себе не одну тысячу особей этого паразита. Им заражена треть всего населения Земли; в некоторых районах Европы носителями являются почти все поголовно.
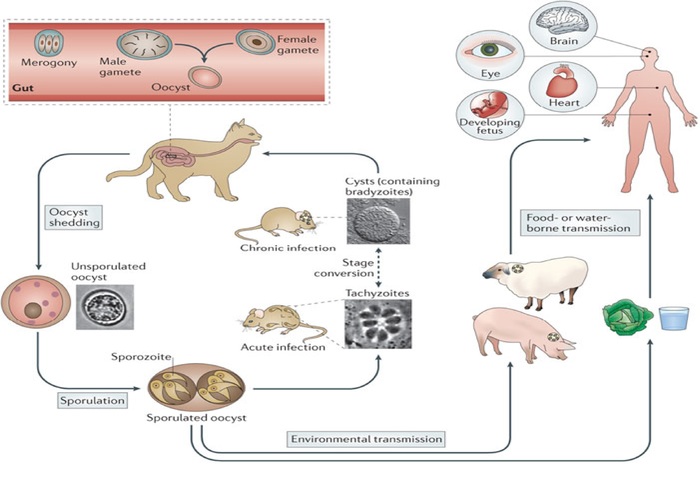
Хотя носителями токсоплазмы являются миллиарды людей, на самом деле человек — не настоящий ее хозяин. Обычный жизненный цикл этого паразита включает кошек, домашних и диких, и животных, которыми питаются кошки. Кошки выделяют яйцеподобные ооцисты токсоплазмы с фекалиями; после этого ооцисты могут много лет ждать в земле, пока не будут подобраны каким-нибудь другим животным—птицей, крысой или газелью. В новом хозяине ооцисты оживают, и простейшие начинают путешествовать по телу в поисках клетки, которую можно сделать домом.
Токсоплазма — близкий родич плазмодия, простейшего, вызывающего малярию. Она также имеет на кончике приспособление, позволяющее ввинчиваться в клетку, но если плазмодий может жить только в клетках печени и позже в эритроцитах, то токсоплазме, в общем-то, все равно. Она может с удобством устроиться в клетке практически любого типа.
Оккупировав клетку, токсоплазма начинает питаться и размножаться. Разделившись на 128 новых копий, паразит разрывает клетку, и молодые паразиты выходят в свет, готовые оккупировать новые клетки. Через несколько дней образ действий паразита меняется. Теперь вместо того, чтобы внедряться в клетки, он строит плотные оболочки, в каждой из которых скрывается несколько сотен особей Toxoplasma. Время от времени одна из таких цист раскрывается, паразиты выходят, внедряются в клетки и производят потомство. Но новые особи сразу же строят собственные цисты и скрываются в них. Там они будут сидеть годами—до тех пор, пока хозяина не съест кто-нибудь из кошачьих.
Оказавшись в окончательном хозяине, токсоплазма вновь просыпается и начинает делиться. Появляются мужские и женские половые формы. Они спариваются и производят ооцисты — начинается новый жизненный цикл.
Если яйца токсоплазмы проглотит человек—в частице почвы или в мясе зараженного животного, — паразит пройдет в его организме те же стадии быстрого, а затем медленного размножения. Люди едва замечают вторжение токсоплазмы; в худшем случае она ощущается как легкий грипп. После того как паразит удаляется в свою тихую пристань — цисту, — здоровый человек вообще перестает его замечать. Может показаться, что токсоплазма — существо мягкое и не заслуживает упоминания в одном ряду с такими паразитами, как трипаносомы или плазмодии. Однако на самом деле токсоплазма манипулирует иммунной системой хозяина не менее изящно, чем упомянутые виды. Если бы паразиты продолжали бешено размножаться, перемалывая все попадающиеся на их пути клетки, они быстро оказались бы в трупе, а не в живом человеке, но ни одна кошка не станет охотиться на труп. Токсоплазме нужно сохранить своего промежуточного хозяина живым, поэтому она использует для регулирования собственной численности иммунную систему хозяина.
Toxoplasma добивается этого при помощи стратегии, противоположной стратегии Leishmania. Если лейшмания подталкивает иммунную систему к производству Т-лимфоцитов, помогающих в производстве антител, то токсоплазма, напротив, высвобождает молекулы, сдвигающие чаши весов в пользу воспалительных Т-лимфоцитов. Т-лимфоциты размножаются в громадных количествах; макрофаги превращаются в убийц, они гоняются за паразитами-простейшими и разрывают их на части.
Уцелеть в этой охоте могут только те особи токсоплазмы, что спят внутри плотных цист. Время от времени несколько паразитов вырываются из своих цист, чтобы добавить в кровь новую порцию своих молекул и тем самым, подобно вакцине, стимулировать иммунную систему. Макрофаги хозяина, насторожившись, вновь загоняют паразита в цисты. Таким образом, благодаря манипуляциям токсоплазмы, ее хозяин остается здоровым и может сопротивляться болезни, тогда как паразит спокойно сидит в своей цисте и терпеливо ждет попадания в землю обетованную — в организм какой-нибудь кошки.
Токсоплазма становится угрозой человеку лишь в том случае, если уютный мирок, созданный ею, по каким-то причинам рушится. К примеру, зародыш не имеет собственной иммунной системы. Его защищают только антитела матери, проникающие через плаценту. Но материнским Т-лимфоцитам вход в кровеносную систему плода запрещен, поскольку они приняли бы зародыш за гигантского паразита и начали бы борьбу.
Материнские антитела успешно справляются с вирусом гриппа или бактерией Escherichia coli, но не могут защитить от токсоплазмы. Для этого необходимы воспалительные Т-лимфоциты, которые загнали бы паразита в цисты. В результате для женщины во время беременности заражение токсоплазмой очень опасно. Если паразит сумеет проникнуть через плаценту в плод, он начнет бешено размножаться. Он попытается включить иммунную систему, которая обуздала бы процесс, но внутри плода некому услышать его зов. Токсоплазма будет бесконтрольно размножаться, пока не вызовет обширное и часто фатальное поражение головного мозга.
В 1980-х гг. токсоплазма научилась убивать при случае еще один тип человека-хозяина — больных СПИДом. Вирус иммунодефицита человека — ВИЧ, причина СПИДа, — проникает в воспалительные Т-лимфоциты и использует их для размножения, убивая при этом. Когда токсоплазма внутри больного СПИДом выходит из цисты и начинает делиться, она ожидает встретить мощный иммунный ответ и рассчитывает, что реакция организма заставит ее вновь спрятаться в укрытие. Но в организме больного почти не остается воспалительных Т-лимфоцитов, и хозяин оказывается беззащитен перед паразитом, как младенец в утробе матери. Паразит начинает бешено размножаться, вызывая поражение мозга. У хозяина начинается расстройство сознания, и в некоторых случаях наступает смерть.
Более десяти лет врачи ничего не могли сделать, чтобы остановить буйство Toxoplasma среди больных СПИДом. Но в 1990-х гг. ученые создали лекарства, способные замедлять ВИЧ и, соответственно, сохранять Т-лимфоциты в организме больного. Тем относительно немногим, кто может позволить себе эти лекарства, токсоплазма больше не угрожает: под действием армии здоровых Т-лимфоцитов паразит с готовностью убирается в свое логово. Но миллионам больных, которые не могут приобрести эти дорогие лекарства, по-прежнему грозит безумие — результат деятельности этого упорного паразита.
Отрывок из книги Карла Циммера "Паразиты: тайный мир".
Предыдущая часть:
НеПаразиты. Часть 5. Иммунитет
Начало серии:
Паразиты. Часть 1. Первое знакомство и осознание