Выдающиеся неметаллы
Просто самый-самый-самый
Углерод
Шестой элемент периодической системы входит в состав всех живых молекул. Его способность образовывать длинные цепочки незаменима для создания молекул ДНК и сложных белков.
Так же человечеству известно несколько десятков миллионов соединений, которые образованы с участием углерода. Что уж говорить, если ему посвящен отдельный раздел химии — органическая.
1️⃣ В природе встречается несколько аллотропных соединений (например, графит, алмаз), но человек создал еще несколько модификаций кристаллической решетки: графен , лондейслит, фуллерен, нанотрубки.
2️⃣Самый тугоплавкий: плавится при 3370 ºC, может поэтому первые нити накаливания в лампах были из бамбука?
3️⃣Способен в естественных условиях, под действием азота и космического излучения, образовывать радиоактивный углерод-14. Благодаря ему люди могут определять возраст археологических, палеонтологических, антропологических находок.
Самый распространённый в земной коре элемент
Кислород
На его долю приходится около 47 % массы твёрдой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе). Это третий по распространенности во вселенной элемент после водорода и гелия.
Чистый кислород — газ, в котором каждая молекула состоит из двух атомов, не имеет цвета, запаха. Под действием электрических разрядов образует аллотропное соединение из трех атомов: озон, обладающее свежим, приятным запахом, который мы чувствуем после грозы.
Озон в высоких концентрациях ядовит, на этом свойстве базируется работа озонаторов, которые обеззараживают воздух.
Жидкий кислород(при низких температурах) имеет светло-голубой цвет, а твёрдый(при низких температурах) представляет собой кристаллы светло-синего цвета. Является парамагнетиком, в жидком виде притягивается магнитом.
Кстати, смесь жидкого кислорода и жидкого озона — один из самых мощных, дешевых и экологичных окислителей ракетного топлива.
Самый фотоактивный
Селен
Хрупкий, блестящий неметалл, названный в честь вечного спутника Земли — Луны. При разном строении кристаллической решетки, количестве атомов, бывает разных цветов: от красного, до черного.
В 1873 году Уиллоуби Смит обнаружил, что электрическое сопротивление серого селена зависит от освещённости, это свойство стало основой для чувствительных к свету ячеек.
Сейчас одним из важнейших направлений являются изучение полупроводниковых свойств как самого селена, так и его многочисленных соединений (селенидов), их сплавов с другими элементами, в которых селен стал играть ключевую роль. В современной технологии полупроводников применяются селениды многих элементов, например, селениды олова, свинца, висмута, сурьмы, лантаноидов.
Человеку селена требуется в день немного, всего около 100 мкг, но без этого количества организм поломается, ведь более 200 ферментов человека содержат в своем составе этот микроэлемент. Селен помогает предотвращать образование свободных радикалов и развитие рака.
Самый маленький и легкий атом
Водород
Одноатомная форма водорода — самое распространённое химическое вещество во Вселенной, составляющее примерно 75 % всей барионной массы.
У этого уникального элемента даже изотопы имеют собственные названия: 1H — протий, 2H — дейтерий и 3H — тритий (радиоактивен).
Массовая доля водорода в земной коре составляет 1 % , однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17 %. Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода.
В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений.
Кстати, вы знали что ¾ промышленного водорода человечество получает из природного газа, а почти все остальное из угля?
И еще, ученых очень интересует металлическая форма водорода, ведь это был бы новый сверхлегкий металл для нашей промышленности.
Самый сильный окислитель
Фтор
Как простое вещество это газ бледно-жёлтого цвета с резким запахом, напоминающим озон или хлор, а при криогенных температурах представляет собой жёлтую жидкость.
При его высокой концентрации загораются даже вода и благородная платина. Не реагирует только с гелием, неоном, аргоном, азотом.
Очень высокая эффективность фтора вызывала значительный интерес к нему и его соединениям. На заре космической эры существовали программы исследования фторсодержащих видов ракетного топлива, однако продукты горения с фторсодержащими окислителями токсичны, поэтому топлива на основе фтора не получили распространения в современной ракетной технике.
Фтор является жизненно необходимым для организма элементом, может вы удивитесь, но основным источником поступления фтора в организм человека является питьевая вода.
В организме человека преобладающая концентрация фтора содержится в эмали зубов в составе и в костях.
Самый распространённый галоген в земной коре
Хлор
Это газ желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом.
Хлор еще один супер активный элемент, который никогда не бывает в природе в свободной форме. Но люди научились получать чистый хлор, и одним из первых его применений стало - отравляющее вещество, использованное в Первую мировую.
Позже отравляющие свойства хлора нашли мирное применение: на его основе стали делать дезинфицирующие средства, отбеливатели. В сочетании с кислородом и калием хлор входит в состав салютов, фейерверков.
Без хлора невозможны многие процессы, проходящие внутри живых клеток. Он участвует в жизнедеятельности в виде ионов и соединений, например, соляной кислоты, которая переваривает пищу в желудке. Ежедневно человеку необходимо до 2,5 грамм хлора. Правда получить суточную норму просто: галоген содержится почти во всех продуктах. Поваренная соль - вообще соединение натрия и хлора.
Самые коварные изотопы, но, которые тоже спасают жизни
Йод
Известны 37 изотопов йода с массовыми числами от 108 до 144. Из них только один (127) является стабильным, период полураспада остальных составляет от 103 мкс до 1,57⋅10^7 лет.
Самый нам известный радиоактивный нуклид 131 распадается с испусканием β-частиц, а также с излучением гамма-квантов.
Так как радиоактивные изотопы биохимически не отличаются от стабильных, то почти весь радиоактивный йод, как и обычный, концентрируется в щитовидной железе, что приводит к её облучению и дисфункции.
Но, при этом, именно это же свойство радиоизотопов йода позволяет использовать его для борьбы с опухолями щитовидной железы и диагностики её заболеваний.
Вот такой вот дуализм.
Самая низкая температура кипения
Гелий
Элемент является вторым по распространенности в космосе, но на Земле его относительно мало.
Гелий - инертный газ и крайне неохотно участвует в создании соединений, так же он не накапливается в атмосфере, потому что гравитации Земли недостаточно, чтобы предотвратить его постепенную утечку в космос. Именно поэтому практически весь наш земной гелий не является изначальной составляющей планеты, он образовался в результате радиоактивного распада. Альфа-частицы, испускаемые ядрами тяжелых радиоактивных веществ, представляют собой ядра изотопа He-4.
He-4 уникален тем, что обладает двумя жидкими формами. Обычная называется гелий I и существует при температурах от точки кипения 4,21 К до около 2,18 К. Ниже 2,18 K форма называется гелий II, она обладает сверхтекучестью: вязкость настолько низкая, что не может быть измерена. Гелий II растекается в тонкую пленку на поверхности любого вещества, которого касается, и эта пленка течет без трения даже против силы тяжести.
В следующем выпуске Выдающиеся орхидеи!
Мне уже многие указывали на появляющиеся неточности, я нашел выход. Вы можете ЗАРАНЕЕ просмотреть и прокомментировать весь материал. Я его теперь предварительно выкладываю в Телеграм. Одна голова хорошо, а две - лучше, значит и контент для Пикабу повысится качеством.
Учёные поняли, почему некоторые кометы светятся зеленым
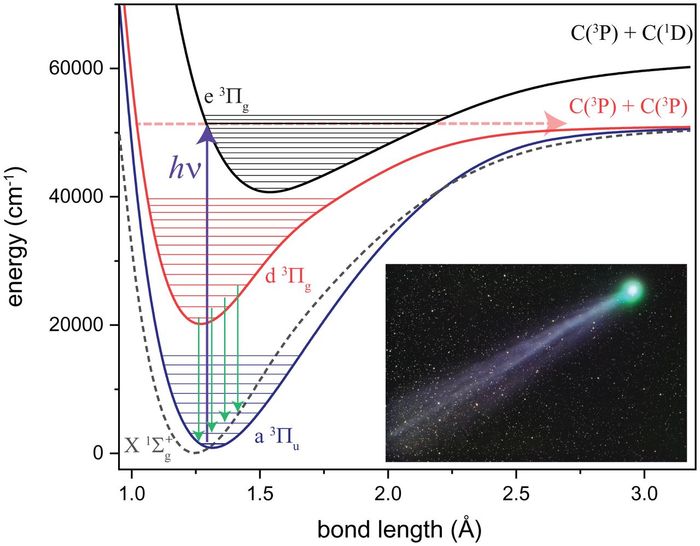
В 2014 году комета Лавджоя пронеслась мимо Земли, ученые заметили у неё зеленую «ауру» — её наблюдали раньше и у других комет. Благодаря первым в своем роде лабораторным измерениям, исследователи выяснили странную химию, стоящую за этим красочным свечением.
Ученые давно подозревали, что зеленое свечение вокруг некоторых комет происходит из-за распада диуглерода.
Чтобы проверить это в лабораторных условиях, исследователи использовали ультрафиолетовый лазер. Это позволило удалить атомы хлора из молекул хлорида кальция (C2Cl4), а оставшуюся молекулу диуглерода облучили высокоинтенсивным светом.
Удивительно то, что вместо поглощения одного фотона света и испускания другого при разрушении молекулы (с частотой, соответствующей зеленому цвету), молекула поглотила два фотона. Один из этих фотонов возбуждает молекулу диуглерода до полустабильного состояния, а второй переводит ее в более высокоэнергетичную и еще более нестабильную конфигурацию. После этого молекула распадается и излучает характерный тот самый «зелёный» фотон.
При этом молекула диуглерода претерпевает два перехода, которые обычно считают «запрещенными». Нужно уточнить, что эти переходы не являются абсолютно запрещенными с точки зрения законов физики, однако они крайне редко наблюдаются в лаборатории.
Дело в том, что в лабораторных условиях молекулы расположены слишком близко друг к другу. Однако в глубоком космосе вблизи комет молекулы расположены на большем расстоянии друг от друга и мало взаимодействуют с другими молекулами или атомами.
Согласно данным эксперимента, на расстоянии от Земли до Солнца время жизни молекулы диуглерода составляет чуть меньше 2 дней. Это помогает объяснить, почему зеленое свечение, связанное с распадом молекулы, появляется только вокруг головы кометы и никогда в ее хвосте — распад происходит слишком быстро.
Исследование опубликовано в журнале Proceedings of the National Academy of Sciences (https://www.pnas.org/content/118/52/e2113315118)
Как подготовить машину к долгой поездке
Взять с собой побольше вкусняшек, запасное колесо и знак аварийной остановки. А что сделать еще — посмотрите в нашем чек-листе. Бонусом — маршруты для отдыха, которые можно проехать даже в плохую погоду.
Хочу все знать #285. Как это работает: радиоуглеродный анализ возраста археологических находок.
Коротко и доступным языком вы узнаете, как ученые узнают возраст той или иной древней находки. И по ныне этот метод сейчас остается самым востребованным.
Как ты знаешь, углерод — главный элемент органики. Возможно, ты даже слышал, что его запасы хранятся в виде стабильных изотопов 12С и 13С (период полураспада отсутствет) и радиоактивного 14С. Последний возникает в атмосфере под действием космических лучей (просто поверь или где нибудь проверь).
От обычных атомов изотопы отличаются числом нейтронов (т.е те же 12, 13, 14..и т.д.), кроме 12-го и 13-го все остальные делают изотоп слегка радиоактивным, но на химические свойства не влияют.
К слову: изотопов у углерода насчитывается 16. А именно с 8С по 23С.
8....23 это ничто иное как атомная единица массы (а.е.м.) и только 12-й и 13-й стабильны.
Поэтому с пищей и воздухом звери, растения и люди усваивают эти формы углерода. Когда флора и фауна испускают дух, вещества в них больше не поступают. В итоге стабильные изотопы остаются целехонькими, а 14С в определенном темпе распадается.
В середине прошлого века химику Уилларду Либби пришло на ум, что, подсчитав соотношение стабильных и радиоактивных изотопов, можно не только установить возраст археологической находки, но и получить Нобелевскую премию.
Оба предположения оправдались. Так как изотоп 14С можно увидеть невооруженным глазом только будучи сильно пьяным (*химическая шутка), для его обнаружения используют масспектрометр — прибор для разделения атомов по их массам.
Чем меньше в очередной окаменевшей матрешке осталось 14С, тем образец старее. А с учетом скорости распада можно довольно точно вычислить дату подделки. Правда, желательно, чтобы возраст находки не превышал 40 - 60 тысяч лет.
А вот как это происходит в лабораториях, увы я не подскажу
Излучение более древних предметов осуществляется с помощью других сравнительных характеристик иных химических элементов.
Да, кстати, нашел 2-х минутный ролик, который наглядно, подробно покажет и расскажет вам об этом методе и очень доступно.
(Рекомендуется для повышения общеобразовательного уровня, а также как тему для первого школьного реферата)
Теперь ты можешь заняться датировкой мумий, валяющихся в кладовке.
Спасибо за внимание!
До встречи в рубрике "Хочу все знать!"
Куда делся углерод из атмосферы Марса?
Геологические данные говорят нам, что в древности климат на Марсе был более теплый и влажный, чем сейчас, из-за наличия более плотной атмосферы, которая в основном состоит из двуокиси углерода. Возникает вопрос: "А куда делся углерод из атмосферы?".
Команда ученых из Калифорнийского технологического института и Лаборатории реактивного движения НАСА попыталась ответить на этот вопрос. Вначале рассматривались два пути ухода углерода. Первый - он оказался "запертым" в горных породах - карбонатах. Второй - он был потерян из-за действия солнечного ветра.
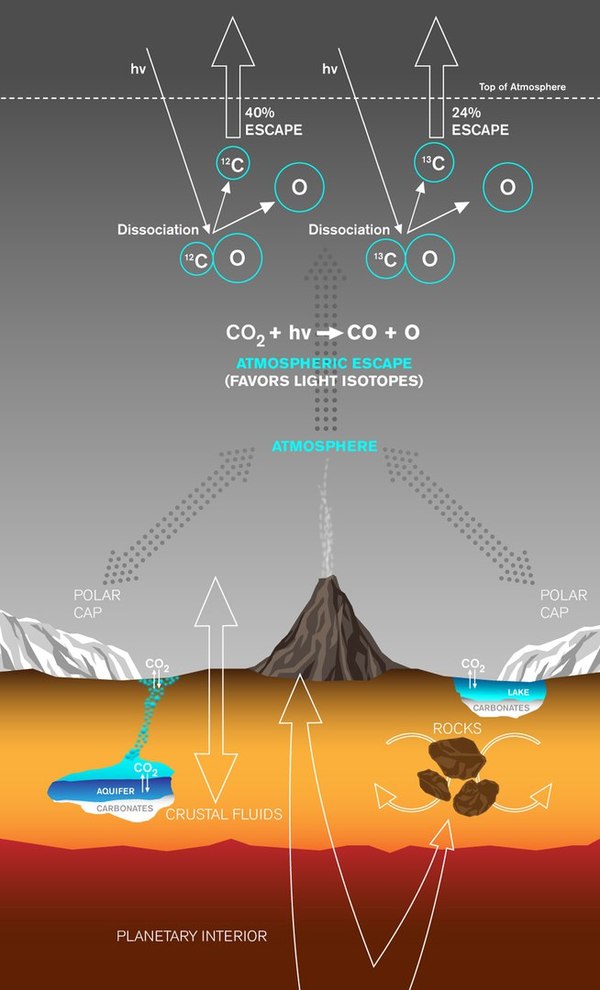
Если работает первый механизм, то на поверхности планеты должны встречаться достаточно большие залежи карбонатов. В августе 2015 года несколько орбитальных аппаратов провели наблюдения и не нашли изобилия карбонатов в верхних слоях коры. Второй механизм тоже был под вопросом - он мог изменить соотношение между двумя изотопами - углерода-12 и углерода-13, которое измеримо. Выходило, что содержание углерода-12 должно ненамного превышать содержание углерода-13 в атмосфере. Однако на деле все оказалось иначе - содержание углерода-13 гораздо выше, чем предполагалось.
В результате был найден другой механизм, который объяснял и потери и "перевес" углерода-13 в атмосфере. Его назвали "ультрафиолетовой фотодиссициацией". Он начинается, когда ультрафиолетовый фотон, испущенный Солнцем, сталкивается с молекулой углекислого газа в верхних слоях атмосферы и "разваливает" ее на окись углерода и кислород. Затем еще один фотон взаимодействует уже с молекулой окиси и "разваливает" ее на углерод и кислород. Некоторые из атомов углерода при этом имеют достаточную энергию, чтобы вылететь за пределы атмосферы, при этом углероду-12 гораздо легче покинуть атмосферу, чем углероду-13. Моделирования показали, что при таком механизме потерь около 3.8 миллиардов лет назад атмосферное давление у поверхности Красной планеты было немного меньше, чем земное в настоящее время.