Лига Химиков
Стабильные радикалы
Обычно в сознании людей слова "радикальный" и "стабильный" воспринимаются как нечто совершенно противоположное. Но в химии возможно все, и стабильные радикалы - не такая уж и диковинка.
Свободный радикал - это частица с неспаренным электроном. Этот электрон может принадлежать как одному атому, так и может быть делокализован (размазан) по всей молекуле. Чем больше у электрона возможностей для делокализации, например, если рядом есть сопряжённые системы двойных связей, ароматические системы, тем стабильнее будет радикал. Ещё устойчивости придают и стерические, т.е. пространственные факторы: если до электрона сложно добраться, то какой бы он ни был реакционной частицей, ему все равно придется прозябать в окружении защищающих его групп. Так один из первых известных стабильных радикалов - трифенилметильный (или тритильный радикал, trityl) - содержит три бензольных кольца, которые одновременно служат площадкой для делокализации, и достаточно объемные, чтобы оградить радикал от нападок других частиц
Ещё одним, и наверное самым распространенным примером будет радикал ТЕМРО (тэмпо), аббревиатуру которого не хочется расшифровать, дабы не ломать психику...
Ладно, хотели - получайте: (2,2,6,6-тетраметилпиперидин-1-ил)оксил.
Этот радикал - стабильное твердое вещество красного-оранжевого цвета. Стабильности ему придает делокализация электрона по N-O связи, плюс еще 4 метильные группы. К слову, монооксид азота NO - тоже радикал. И это ваш кислород - туда же, бирадикал.
TEMPO - самый известный в семействе N-оксильных радикалов. Кроме него стоит упоминания фталимид-N-оксильный радикал, или PINO. Он более реакционноспособен и может жить в растворе в течение нескольких минут. Есть и другие радикалы этого класса, которые настолько стабильны, что их можно поделить на колонке.
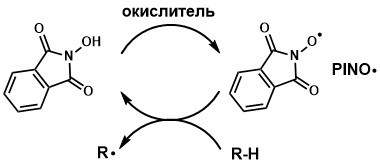
Так выглядит образование фталимид-N-оксильных радикалов под действием окислителей:

Для того, чтобы радикалы можно было использовать в химических реакциях, необходимо найти золотую середину между устойчивостью и реакционной способностью. С одной стороны, радикал должен обладать достаточной энергией, чтобы разрывать и окислять нужные связи. Но чем больше энергия, тем меньше стабильность и разборчивость: велика вероятность, что он накинется на первую попавшуюся связь или прореагирует сам с собой.
По мере реакции радикал расходуется и окраска исчезает:

Если к радикалу добавить какой-нибудь легкоокисляемый субстрат (т.е. вещество, которое будет реагировать), то пино радостно отрывает у него водород, в свою очередь образуется еще один радикал, судьба которого может быть различна. Он может окислиться, прорекомбинировать (соединиться) с другим радикалом, оторвать еще где-то водород, провзаимодействовать с пино...
Собсна, зачем нужны эти радикалы?
Круг их применения широк - от промышленных процессов контролируемой полимеризации до тонкой химии. Устойчивые радикалы могут добавлять в качестве стабилизаторов в легкоокисляемые вещества, чтобы обрывать цепочку радикальных реакций.
Часто их используют в качестве медиаторов окисления или катализаторов, в фотохимических процессах.
ТЕМРО - известная "радикальная ловушка", то есть он может перехватывать другие радикалы, образующиеся в реакции, тем самым тормозя ее. Такой прием можно использовать, чтобы выяснить, радикальный ли механизм процесса (но не со 100% гарантией). Ещё одна радикальная ловушка - ВНТ. Его можно также встретить в разной косметике, где он играет роль антиоксиданта.
Стабильные радикалы удобно анализировать по ЭПР (электронный парамагнитный резонанс), что дает возможность использовать их в качестве спиновых меток для детектирования различных биомолекул.
И да, стабильные радикалы в каком-то смысле спасают нам жизнь. Поскольку в каждом живом существе постоянно идут процессы синтеза/окисления, параллельно могут образовываться свободные и очень активные радикалы, которые повреждают все на своем пути. И тут на помощь приходят вещества, которые принимают удар (а вернее, электрон) на себя. Бета-каротин и каротиноиды, витамин Е и всякие штуки, называющиеся антиоксидантами - они могут образовывать радикалы с низкой энергией которые безопасны для нас, ходячей органики.
А вы думали, это для красоты растения цветные. Неа, просто куча сопряжённых двойных связей создаёт именно такой уровень энергии, при котором поглощается видимый свет. Но это уже другая история.
Кристаллы фенола
Фенол. Расплавление кристаллов теплотой дыхания. Микроскоп МИН-8, поляризация, скрещенные поляризаторы, объектив 9х. Кристаллы фенола образованы на предметном стекле путем кристаллизации из раствора фенола в ксилоле. Видно, как тают кристаллы при дыхании на них.
Туповатый вопрос
У меня давеча возник вопрос(не силен в химии) Почему H2O если это соединение водорода и кислорода не обладает свойством гореть?
Просьба не бить грязными тряпками
Крутой дед-химик показывает 25 экспериментов за 15 минут
Смотрите до конца!))