В лаборатории созданы органоиды, содержащие клетки мозга с генами неандертальцев
Исследователи создали крошечные мозгоподобные органоиды – комочки, состоящие из помещенных в питательный раствор клеток мозга.
Эти клетки содержат гены двух родственных современному человеку исчезнувших видов: неандертальцев и денисовцев.
Ткани, созданные генно-инженерными методами из стволовых клеток человека, далеки от того, чтобы быть настоящим воплощением мозга давно несуществующих видов людей.
Однако, они демонстрируют явные отличия от органоидов из клеток современного человека, включая размер, форму и текстуру.
Результаты, опубликованные 11 февраля в Science, могут помочь ученым понять генетические пути, позволившие эволюционировать человеческому мозгу.
«Это необычная статья с некоторыми экстраординарными утверждениями» - сказал Грэй Кэмп, специалист по биологии развития из Базельского университета в Швейцарии, чья лаборатория сообщила в прошлом году о растущих органоидах мозга, содержащих общий для людей и неандертальцев ген.
Опубликованная работа продвигает исследование дальше, рассматривая генетические варианты, утерянные людьми в ходе эволюции.
Но Кэмп остается настроенным скептическим относительно последствий полученных результатов и говорит, что работа ставит больше вопросов, требующих исследований.
Люди являются гораздо более близкими родственниками неандертальцев и денисовцев, чем любых существующих приматов. Около 40% неандертальских генов все еще присутствует среди современных людей.
Но доступные специалистам средства изучения мозга этих древних видов ограничены. Мягкие ткани плохо сохраняются и большинство исследований полагаются на изучение размера и формы окаменелых черепов.
Знание того, как гены вымерших видов человека отличаются от современных, помогает ученым понять, что именно делает наш вид уникальным, особенно в том, что касается мозга.
Группа исследователей под руководством нейробиолога из Калифорнийского университета в Сан-Диего Элиссона Муотри использовала технологию редактирования генома CRISPR-Cas9 чтобы ввести ген неандертальцев и денисовцев, названный NOVA1 в плюрипотентные* стволовые клетки человека.
*Такие клетки могут развиться в любой другой тип клеток.
Ученые культивировали измененные стволовые клетки чтобы сформировать органоиды – скопления мозгоподобной ткани размером до 5 миллиметров в поперечнике.
При их сравнении с органоидами настоящей мозговой ткани человека стало видно, что вариант с геном NOVA1 выглядит иначе.
Органоиды человеческого мозга обычно гладкие и имеют форму сферы, а полученные генетической модификацией скопления тканей имели неровные, сложные поверхности и были меньшего размера.
Вероятно, причина в том, что эти клетки росли и размножались иначе.
Генетическое сравнение.
Чтобы определить, какой древний ген следует экспрессировать в органоидах, исследователи сравнили библиотеку генетических последовательностей человека с почти полными геномами двух неандертальцев и одного денисовца. Специалисты обнаружили 61 ген, который у всех современных людей отличается от его древних версий. Среди них NOVA1, который участвует в формировании мозговых синапсов - соединений нервов, и ассоциирован с неврологическими заболеваниями при изменении его активности.
Человеческий ген NOVA1 отличается от своего древнего варианта, все еще представленного у других живущих сейчас приматов, единственным азотистым основанием, которое исследователи отредактировали в стволовых клетках при помощи технологии CRISPR-Cas9. Эта разница влияет на единственную аминокислоту в белке NOVA1, производимом древними органоидами. «Факт того, что все или почти все люди имеют новую версию этого гена, означает, что на каких-то этапах эволюции такое изменение дало огромные преимущества. Вопрос в том, что это за преимущества» - сказал Муотри.
Различия между полученными органоидами продолжаются на молекулярном уровне. Команда ученых выявила 277 генов, активность которых отличается в органоидах с древними генами и с генами современного человека. Некоторые из этих генов известны своим влиянием на развитие нейронов и связей между ними. В результате архаичные органоиды содержали другие уровни синаптическИХ протеинОВ и картина возбуждения их нейронов выглядит менее организованно, чем у контрольных тканей. Также имеются свидетельства, что они быстрее созревали.
Большая разница.
«Наиболее значимое открытие в том, что вы возвращаете ген в его раннее [наследственное, родовое, свойственное роду] состояние, и видите эффект на органоиде» - сказал Вольфганг Энард, эволюционный генетик в мюнхенском университете Людвига Максимилиана. Он поражен, что такая маленькая генетическая разница вызывает настолько очевидные изменения. Но он скептичен относительно того, что странный вид органоидов многое говорит нам о мозге неандертальцев.
Грэй Кэмп также предупреждает, что едва ли эти созданные на основе древних генов органоиды полностью представляют настоящие неандертальские ткани. По его мнению, наблюдаемые свойства могут быть результатом изменения важного белка, содержащегося в человеческом организме. Совместные эффекты многих мутаций всё время накладываются друг на друга. Это как карточный домик. Вы меняете одну аминокислоту и всё ломается. Мозг перестает работать.
И всё-таки, способ с редактированием органоидов может быть применим для изучения эволюции мозга приматов, считает Сюзанна Херкулано-Хузель – эволюционный нейробиолог из университета Вандербильта в Нэшвилле, Тенесси. Команда Муотри планирует создать органоиды, измененные таким образом, чтобы содержать другие архаичные гены, которые могли бы пролить свет на загадки человеческого мозга. Если ученые смогут понять эволюционные пути, приведшие человека к его нынешнему состоянию, то, возможно, они лучше поймут заболевания, специфичные для мозга человека.
Как исправить человека. CRISPR/Cas9: новейшая система генной модификации, которая обещает изменить нашу жизнь
Фантастические, пугающие многих истории о вмешательстве в человеческий геном долгие годы оставались именно фантастическими. Практичных методов изменить ДНК, с добрыми или иными намерениями, не существовало. Но теперь такой метод есть: заимствованная у бактерий система CRISPR/Cas9 позволяет вести генетическую модификацию любых организмов с такой точностью и эффективностью, о которой прежде можно было лишь мечтать. И вот уже китайские медики объявили о планах первого целенаправленного редактирования ДНК человека. Вмешательство в наш геном уже не фантастика. Но так ли это пугает?
Иммунитет
– естественный «иммунитет» бактерий, биохимическая система защиты от вирусов, которая требуется одноклеточным организмам, неспособным поддерживать такую сложную иммунную систему, как наша. Первые намеки на ее существование были найдены еще в конце 1980-х, когда Йошизуми Исино и его коллеги исследовали обыкновенную кишечную палочку, точнее говоря, один ее малопримечательный ген (iap).
На всякий случай японцы секвенировали его последовательность вместе с участками по бокам от него: может, там будут какие-то фрагменты, участвующие в регуляции активности iap?.. Вместо этого биологи обнаружили в ДНК длинные последовательности повторяющихся, совершенно идентичных повторов длиной ровно 29 нуклеотидов. Между ними – как сухие растения между листами бумаги в гербарии – оказались «проложены» короткие фрагменты длиной по 32 нуклеотида, которые не повторялись никаким образом.
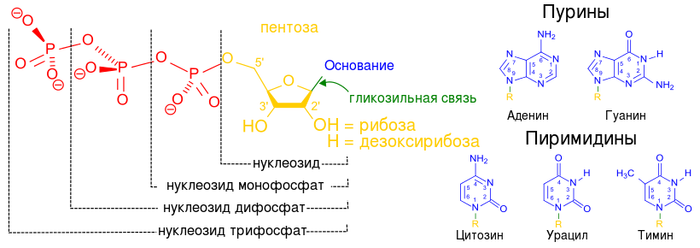
Строение нуклеотидов / ©wikipedia
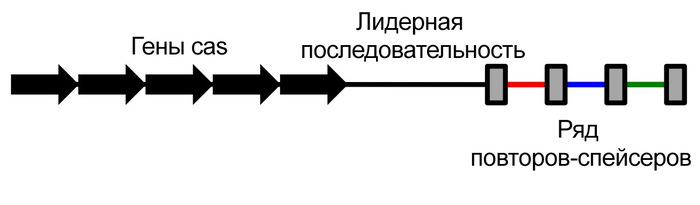
Позднее эту странную часть ДНК назвали «регулярно сгруппированные, разделенные короткие палиндромные повторы» – Clustered Regularly Interspaced Short Palindromic Repeats. В остальном работы над ними надолго остановились, хотя многие ученые заинтересовались загадочными участками хромосомы, а некоторые даже рассуждали об их роли. Функциональное значение CRISPR оставалось загадкой, да и особенных прорывов никто от них не ждал: «Биологическое значение этих последовательностей неясно», – написал тогда Исино с соавторами.
Однако во второй половине 1990-х начался настоящий бум секвенирования. Установить последовательность ДНК становилось все проще, и геномы все новых и новых организмов стали пополнять компьютерные базы данных и анализироваться со всех сторон. Таинственная – и вроде бы бессмысленная, совершенно не похожая ни на какой ген – последовательность CRISPR обнаруживалась у бактерий повсеместно. Нидерландский биолог Рууд Янсен заметил, что они всегда соседствуют с генами одних и тех же белков. Функции их тогда были тоже неизвестны, и их назвали просто «белками, ассоциированными с CRISPR» (CRISPR-Associated Proteins, Cas).
Упрощённая схема строения CRISPR / ©wikipedia
И лишь в 2005 году сразу три группы исследователей сообщили, что уникальные участки CRISPR – это фрагменты вирусных геномов. «Тут у меня что-то щелкнуло», – вспоминал впоследствии всемирно известный биоинформатик и эволюционист Евгений Кунин. К тому времени он уже несколько лет бился над загадкой CRISPR – и, наконец, его озарило: эта ДНК может быть частью противовирусной защиты бактериальной клетки.
Эта идея понравилась микробиологу Родольфу Баррангу, который в то время работал в компании Danisco, производящей йогурты. В этом бизнесе вирусная эпидемия среди молочнокислых бактерий способна принести серьезные убытки, и исследователь искал методы защиты от нее. Чтобы проверить гипотезу Кунина, он заразил стрептококков Streptococcus thermophilus двумя штаммами бактериофагов. Большинство бактерий погибло, однако выжившие оказались довольно устойчивы к этим вирусам. Секвенировав их ДНК, ученые подтвердили: в ней появились следы встречи.
Инструмент
Дженнифер Дудна и Блейк Виденхефт взялись за изучение структуры белков Cas: к этому моменту выяснилось, что они выполняют роль нуклеаз, то есть разрезают ДНК. Несмотря на все находки, значение открытия по-прежнему было неясным: «У вас нет никакой определенной практической цели, – объясняла Дудна работавшему в ее лаборатории Виденхефту. – Важно лишь понять, как это работает». Но по мере работы выяснились многие удивительные детали.
CRISPR – это, действительно, нечто вроде гербария, каталог, в котором бактериальная клетка сохраняет образцы, фрагменты геномов вирусов, с которыми доводилось сталкиваться ей или ее предкам. Пользоваться этим каталогом могут специальные белки, ассоциированные с CRISPR (CRISPR-Associated Proteins, Cas). Ориентируясь на эти образцы, они быстро распознают новые вирусные гены и разрезают их, выводя из строя.
Биолог Карл Циммер объясняет работу системы CRISPR/Cas так: «По мере того, как область CRISPR заполняется вирусной ДНК, она становится ключевой «галереей» в клетке, где представлены «портреты» микробов, с которыми бактерии доводилось встречаться. Впоследствии эта вирусная ДНК может использоваться для «наведения» точного орудия Cas-белков».
Для этого бактериальная клетка синтезирует на сохраненных фрагментах ДНК короткие образцы, молекулы РНК. Каждый из этих РНК-«гидов» (гРНК) связывается с белком Cas, способным разрезать ДНК, подходящую под этот образец. Эти комплексы постоянно патрулируют клетку, отслеживая появление любой ДНК и сопоставляя ее с гРНК. Если совпадение есть, двойная спираль ДНК тут же разрезается на части и инактивируется. «Как только мы осознали Cas в качестве программируемых, разрезающих ДНК ферментов, произошел интересный момент, – вспоминала впоследствии Дженнифер Дудна. – Мы воскликнули: «Боже, да это же может быть инструментом!»»
Сегодня определено целое семейство белков Cas, но наиболее изученным и освоенным оказался протеин Cas9, выделенный из бактерий Streptococcus pyogenes – возбудителей скарлатины. Именно он лег в основу новейшей методики генетической модификации живых организмов CRISPR/Cas9, методики, обещающей невиданный прорыв в биотехнологиях, сельском хозяйстве и медицине.
Палиндромы в ДНК: A. Палиндром, B. Кольцо, C. Стебель / ©wikipedia
Модификация
В самом деле, белок Cas9 – это нуклеаза, то есть фермент, разрезающий ДНК. Для любого метода генетической модификации – удаления или добавления целевых активных генов в организм – эта способность играет ключевое значение. Чтобы копировать и вставлять, нужно вырезать, причем делать это в строго определенном месте. До сих пор с точностью у генетиков были проблемы.
Вспомним, что молекула ДНК – это, по молекулярным меркам, невероятно длинная цепочка, общая длина которой в каждой хромосоме каждой нашей клетки достигает порядка сантиметров. Разнообразием этот полимер не отличается, состоя всего из четырех разных звеньев: аденина (А), гуанина (Г), тимина (Т) и цитозина (Ц), которые повторяются миллионы и миллионы раз. Найти в этом однообразии именно нужный участок неимоверно сложно.
Кристаллическая структура S. aureus Cas9 в комплексе с сгРНК и её целевой ДНК / ©wikipedia
Долгое время в распоряжении генетиков имелись лишь системы с нуклеазами, которые распознавали короткие участки – например, четыре нуклеотида АТЦЦ или ТГЦА, – которых на протяжении цепочки могут встречаться десятки и сотни. В результате разрезы производились в случайном из этих мест, и лишь кропотливая работа позволяла отобрать клетки, в которых этот процесс прошел в нужном участке генома. В отличие от них, вооруженный гРНК белок Cas9 распознает фрагмент длиной с эту РНК – около 20 нуклеотидов. Такие участки уже, как правило, вовсе не повторяются в ДНК даже высших организмов.
Более того, сама структура комплекса Cas9 с гРНК определяет простоту работы с ней. Достаточно открыть в компьютере базу с ДНК нужного организма, найти фрагмент, который должен быть разрезан, и синтезировать молекулы гРНК с той же последовательностью оснований (и заменой тимина, роль которого в РНК играет урацил, У). Cas9 – нуклеазы неразборчивые и будут резать ДНК где угодно, лишь бы гРНК совпала.
Кристаллическая структура Cas9, связанного с ДНК / ©Nature
В отличие от этого, системы генетической модификации предыдущих поколений требовали долгой работы по проектированию и синтезу ферментов-нуклеаз, способных распознавать определенные участки ДНК. Например, методы с использованием связывающихся с ДНК «цинковых пальцев» ZFN (Zinc Finger Nuclease) или белков TALEN (Transcription Activator-Like Effector Nucleases) теоретически позволяют работать с еще более длинными фрагментами ДНК. Однако для каждой конкретной задачи их приходится проектировать отдельно.
Наконец, CRISPR/Cas9 универсален по отношению к разным видам модифицируемых организмов. Метод прост и эффективен и, по крайней мере, теоретически с одинаковым успехом подходит для получения риса с повышенным содержанием витамина А или лосося, набирающего массу вдвое быстрее обычного, для внесения новых генов или замены дефектных у племенных лошадей и людей… Но прежде чем перейти к людям, давайте «потренируемся на кошках». А лучше – на мышах.
Мыши, люди и все-все-все
Представим, что нам требуется получить мышей-альбиносов, чтобы изучить, как влияет это состояние на здоровье разных систем организма у людей. Для этого следует «выключить» обе копии гена, связанного с синтезом пигмента меланина. Если мы привержены традиционным подходам к генетической модификации (кстати, по большей части тоже заимствованным у бактерий), то нам стоит запастись терпением.
Для начала нам следует синтезировать «ген альбиносости» и получить мышиные эмбрионы на самых первых этапах развития. Затем в их ядра через тончайшую полую стеклянную иглу внести новую ДНК. В делящихся клетках происходит рекомбинация – обмен гомологичными участками хромосом – так что, трижды сплюнув, будем надеяться, что она захватит и нужный нам фрагмент. Методом проб и ошибок, бесконечными повторами и отбраковыванием мы можем получить мышей, которые получили одну копию «гена альбиносости» и оказались способны передать ее потомству. Затем, скрещивая таких животных, рано или поздно мы добьемся рождения особей с заменой обеих копий. Можно выжидать, а лучше сразу переходить на CRISPR/Cas9.
Лабораторная мышь-альбинос / ©National Geographic
Действительно, чтобы получить тех же мышей-альбиносов, достаточно найти пограничные участки нашего целевого гена и синтезировать для них гРНК, после чего ввести в эмбрион вместе с белками Cas9 и ДНК нового гена. Подхватив гРНК, нуклеазы Cas9 разрежут обе копии гена по краям, после чего в дело включатся клеточные системы репарации, ответственные за поддержание целостности генома.
Это чрезвычайно ответственная задача, поэтому белки репарации действуют быстро и даже грубо. Обнаружив повреждение ДНК – тем более такое опасное, как двухцепочечный разрез, – они готовы подхватить первый попавшийся кусок ДНК, буквально «затыкая» образовавшуюся брешь. Так что если в клетке окажется достаточно нужных нам фрагментов, в место, разрезанное белками Cas9, будут встроены они.
Недаром за прошедшее с момента открытия CRISPR/Cas9 генетическая модификация совершает прорыв за прорывом. Громкое заявление китайских биологов – тому лишь один из примеров. КНР остается страной с одним из самых мягких законодательств в области генной инженерии. Даже в Великобритании, где разрешены эксперименты по применению CRISPR/Cas9 на человеческих эмбрионах, получившихся химер требуется уничтожать в возрасте не старше 14 суток. В Китае дозволяется куда больше.
Такие работы невероятно перспективны: буквально в последние годы показано, что CRISPR/Cas9 позволяет редактировать гены даже во взрослом организме, очищая ДНК Т-лимфоцитов от заразившего их ВИЧ. А в том же Китае ученые (не слишком успешно) пытались получить эмбрионы, устойчивые к этой инфекции. Теперь же речь идет о борьбе с раком. Для этого медики планируют отредактировать ДНК тех же Т-лимфоцитов – точнее говоря, ген белка PD-1, который в норме держит их под контролем.
Т-лимфоцит / ©wikipedia
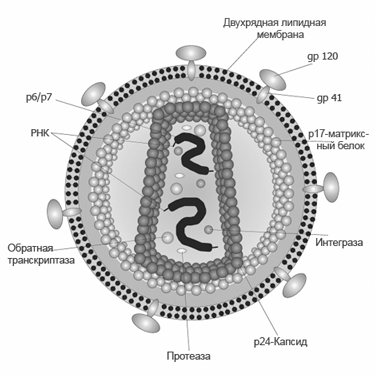
Строение вируса иммунодефицита человека / ©wikipedia
Активный ген PD-1 блокирует способность Т-лимфоцитов атаковать собственные клетки организма и предотвращает развитие аутоиммунных заболеваний. Однако в случае рака такая способность пришлась бы очень к месту, и ученые собираются, забрав клетки у реальных онкологических больных, изменить ген PD-1 с помощью CRISPR/Cas9 (теперь мы в общих чертах понимаем, как это можно сделать). Вернув в организм эти лимфоциты, авторы ожидают, что те начнут размножаться и атаковать опухоль.
Рак и ВИЧ – лишь пара громких примеров. Однако в будущем CRISPR/Cas9 и генетическая модификация позволят избавиться от множества других болезней. Тем более что множество тяжелейших состояний связаны с нарушением в работе всего одного гена: их, видимо, исправить будет куда проще, чем вылечить тот же рак. В отличие от них, доброта и ум, красота или спортивные способности – продукт работы массы разных генов, воспитания и других факторов среды. Так что CRISPR/Cas9 принесет лишь пользу, а использовать ее во вред вряд ли получится. Разве что просто попугать.
Вы хотите головоломок?
Их есть у нас! Красивая карта, целых три уровня и много жителей, которых надо осчастливить быстрым интернетом. Для этого придется немножко подумать, но оно того стоит: ведь тем, кто дойдет до конца, выдадим красивую награду в профиль!
CRISPR/Cas9 [научный фотоконкурс]
И я решила поучаствовать в фотоконкурсе)
Немного о себе: в этом году закончила бакалавра по программе биохимии в Германии. В дипломной работе использовала сейчас довольно модную и известную (ну хотя бы из-за нобелевки в этом году) технологию CRISPR/Cas9.
На первой фотографии нормальные раковые клетки (плотность, безусловно, очень высокая, контроль потом переделывала). На второй - клетки, не способные производить определенный протеин, так как была введена мутация в гене с помощью CRISPR/Cas.
Бонусом - мое новое рабочее место. Продолжаю работать с CRISPR в отделе генотипизирования в институте исследования биологии старения.
Кто будет редактировать гены граждан России?
Нашел на youtube посмотрел все выпуски. Чего и вам советую!
Кто будет редактировать гены граждан России?
Нашел на youtube посмотрел все выпуски. Чего и вам советую!
Что такое CRISPR?
Те из вас, кто старается следить за достижениями в области современной биологии, хотя бы раз наверняка сталкивались с упоминанием загадочной технологии CRISPR, которая вроде как революционировала поле боя молекулярных генетиков. Предполагаю, что даже многие биологи плохо себе представляют, как эта штука работает и какие возможности дает, так что решил запилить пост на эту тему. Сразу скажу, что для понимания содержания статьи потребуется как минимум знать, что такое ДНК. Если надо освежить знания – добро пожаловать в мой прошлый пост.
Итак, встречайте:
CRISPR - Clustered Regularly Interspaced Short Palindromic Repeats (регулярно расположенные группами короткие палиндромные повторы) – это вообще такие участки генома бактерий и архей, отвечающие за любопытную систему защиты от вирусов. Еще в далеком 2013м ученые смогли заставить эту систему работать в искусственно созданных условиях, заставляя ее резать ДНК не в бактериях, а вполне себе в эукариотических клетках. С тех пор много воды утекло, элементы этой системы подпилили до совершенства и коммерциализировали все кому не лень. Но как же оно все работает в лаборатории и помогает ученым? Давайте разбираться.
Одна из задач, которую решают современные молекулярные генетики – зачем нужен какой-то ген. Прочтение генома в наше время – довольно простой процесс, но он даст нам тупо последовательность букв, а не понимание того, какой ген за что отвечает. Классический способ узнать, зачем нужен какой-то ген – вырубить его и посмотреть, что будет. Научным языком это называется «нокаутировать» ген, а полученный организм – «нокаут» по такому-то гену. Далее можно исследовать, что же не так с несчастным животным/растением, и делать выводы о функциях вырубленного гена.
Казалось бы, нормальная мышка, но на самом деле это нокаут по гену RAG1, и у этой мышки нет иммунитета.
И вот очень классно было бы иметь способ, позволяющий просто резать ДНК в ровно нужном тебе месте, вырубая именно тот ген, который надо... В принципе, до прихода CRISPR такие методы существовали (см. TALEN, например), но, как правило, они все были довольно трудоемкими в исполнении. CRISPR же - сравнительно простая технология, применение которой легко поставить на поток. Что же конкретно происходит при ее применении? Чтобы разобраться, давайте сначала введем несколько важных терминов, без которых никак.
Сas9 – бактериальный белок, способный вносить двунитевые разрывы в молекулу ДНК (вы же помните, что там две нити, да?).
Guide RNA, или gRNA – специальная молекула РНК, которая служит как система наведения – она заставляет белок Cas9 резать там, где надо. Напомню, что РНК химически очень похожа на ДНК, но так исторически сложилось, что РНК выполняет в клетке иные функции, чем ДНК.
CRISPR RNA, или crRNA – часть gRNA, отвечающая непосредственно за наведение Cas9 на цель.
Tracer RNA, или tracrRNA – вторая часть gRNA, она отвечает за связывание с белком Cas9. В природе эта и предыдущая штуковина – две отдельные молекулы, но в лабораторных опытах, как правило, используют химерную молекулу, в которой эти половинки просто сшиты друг с другом.
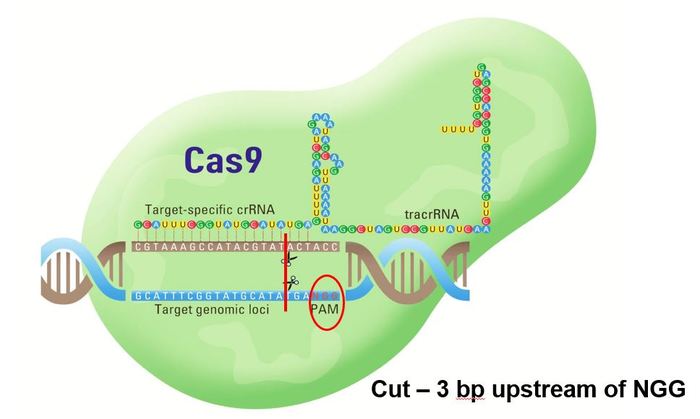
Вот теперь можно переходить к практике. Допустим, ученым надо вырубить ген А в культуре клеток. Культура клеток, кстати – это такая каша из клеток, как правило, одного типа, которая просто растет в специальной емкости в лаборатории. Ученые часто с ними работают, чтобы не париться с настоящими животными и не мучить людей. Так вот, ученым известна последовательность ДНК того самого гена А в этих клетках, и они решают использовать метод CRISPR, чтобы сделать грязное дело. Для этого берется (заказывается у поставщика или синтезируется самостоятельно) молекула gRNA, причем молекула эта подбирается таким образом, чтобы ее кусок – crRNA – был комплементарен тому участку гена А, который надо разрезать. К ней подмешивается белок Cas9 – эдакие безумные ножницы, которые очень любят резать ДНК. Однако сами они резать как попало не могут – им надо показать, где резать – именно это и делает gRNA. Эту смесь из gRNA и Сas9 засовывают внутрь клеток (тут есть разные способы, это отдельная история), где она и приступает к работе. Вторая половина gRNA называется tracrRNA, и за нее белок Cas9 цепляется к gRNA. Благодаря crRNA дружная парочка gRNA+Cas9 садится на нужный участок ДНК клетки и режет обе цепи ДНК. Причем не где-нибудь, а в строго определенном месте – между шестой и седьмой буквой того участка генома, который был комплементарен crRNA. Единственное условие тут – первые три буквы этого участка должны быть NGG, где N – это вообще любая буква. Не хочу излишне пудрить вам мозги, но эти волшебные важные три буквы называются PAM site (Protospacer Adjacent Motif).
Схема работы комплекса CRISPR-Cas9. Зеленая блямба – белок Cas9 – вместе с цветастой молекулой gRNA, состоящей из crRNA и tracrRNA, сел на геномную ДНК в клетке. Красной линией отмечено, где именно Cas9 разрежет двунитевую ДНК – 3 буквы «вверх по течению» от триплета NGG.
И вот тут начинается самое интересное. Заметьте, система CRISPR просто вносит разрез, она больше ничего не умеет! Достаточно ли этого, чтобы вырубить ген в клетке? Никак нет. За миллионы лет эволюции живые системы научились беречь ценную ДНК и исправлять в ней всякого рода разрывы, химические поражения и прочие гадости. Занимается этим специальная клеточная контора под названием система репарации ДНК. Как только она замечает, что имеет место двунитевой разрыв ДНК, на место аварии сразу рекрутируются разные белковые комплексы, которые пытаются исправить ситуацию, причем каждый по-своему. Доходит до того, что они реально конкурируют друг с другом за право починить ДНК, и в итоге существует несколько вариантов развития событий.
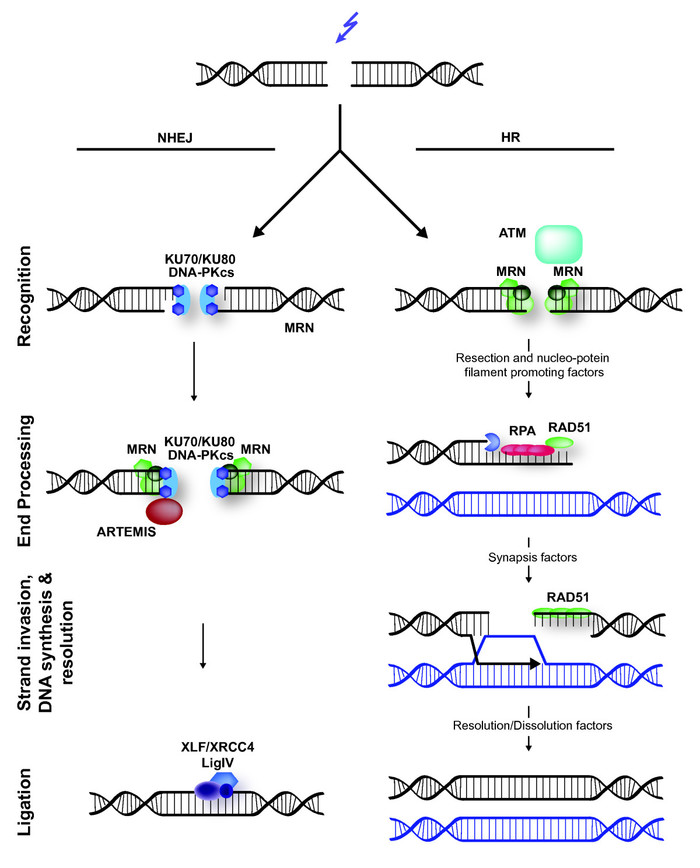
Вариант 1. Процесс идет по пути негомологичного слияния концов – Non-Homology End Joining (NHEJ). Чертова куча белков прилетает на место разрыва, и работает прям как ваш сантехник – одни отрезают чуть-чуть оборванные концы (не всегда, правда), другие достраивают концы как надо, третьи сшивают место обрыва. Удобно, быстро – но не всегда точно!! Во время достраивания концов иногда в последовательности оказываются буквы, которых там изначально не было, причем их количество тоже может варьировать. Извини, начальник, так получилось... Ну а если все сделали как надо – наш комплекс CRISPR-Cas9 никуда не делся, и он опять порежет это место! И так до тех пор, пока рьяные белки-помощники не изменят место разрыва до такой степени, что Cas9 больше не сможет на него сесть. Ну или Cas9 самовыпилится, устав хреначить ДНК.
Вариант 2. Процесс идет по пути гомологичной репарации – Homology Directed Repair (HDR). Тут все еще сложнее: вместо того, чтобы тупо сшить два куска ДНК, попутно вставив пару сомнительных букв, эти белки решают «заглянуть в инструкцию» - в данном случае, во вторую копию этого гена в сестринской хромосоме! Вы ведь помните, что у большинства организмов (включая нас с вами) в каждой клетке содержится две (а то и больше) копии ДНК? На всякий ген есть его гомологичная «сестричка», которая более или менее на него похожа. В случае HDR путем хитрых манипуляций белки используют сестринскую копию гена, чтобы правильно восстановить место разрыва. Этот метод более надежный, чем NHEJ, и дает ученым одно важное преимущество, о котором мы поговорим чуть позже. Напомню, что если системе репарации удалось восстановить исходную последовательность порванной цепи, то ее, беднягу, опять режет Cas9, и все начинается с начала.
Схема путей репарации ДНК. Слева – путь NHEJ, быстрый и неточный. Справа – HDR, использующий гомологичную хромосому в качестве инструкции.
Итак, если мне хочется просто нокаутировать ген в моем объекте исследования, мне достаточно надеяться, что клетка после обработки CRISPR-Cas9 запустит первый вариант репарации (NHEJ), и в итоге часть клеток получит мутации, которые вырубят нужный мне ген. Профит, дело сделано. Но зачем я тогда упоминал про второй вариант репарации, спросите вы? Давайте еще раз на него посмотрим. Белки используют гомологичную копию гена, чтобы исправить повреждение. А что если...(с этого начинаются все безумные идеи ученых)...что если этим белкам под видом гомологичной копии подсунуть кусок ДНК, который мы сами создали, который содержит нужные нам изменения в гене? Тогда они вставят информацию с этого куска в геном в твердой уверенности, что сделали все как надо... Образно говоря, мы слегка подправили им инструкции. И действительно, так и происходит! Такая технология позволяет нам не просто вносить заранее непредугадываемые изменения в ДНК, но и абсолютно точно изменять нужные нам ее участки. Обратите внимание, что CRISPR в этом случае тупо ломает ДНК там где надо, чтобы тем самым вызвать «сантехников», а всю реальную работу делают уже они. С точки зрения лабораторного эксперимента все просто: в этом случае вместе с gRNA и белком Cas9 мы также вводим в клетку кусок ДНК, несущий нужный нам код – он называется донором. В идеальном варианте информация донора в неизмененом виде встроится в целевой геном, добавляя клеткам или организму нужные нам генетические особенности.
Итак, суммируем: для простого нокаута нам достаточно полить клетки/организмы смесью из gRNA и Cas9, чтобы сами клетки при попытке исправить устроенные Cas9 разрушения с помощью механизма NHEJ внесли в ДНК случайные мутации, вырубающие ген. Для точной же модификации ДНК мы также добавим в нашу взрывную смесь донорную последовательность, которую клетки благополучно используют в процессе HDR, чтобы «поправить» свою ДНК (а на деле внести в нее необходимые нам изменения).
Разумеется, такие эксперименты требуют нехилых умственных и временных затрат: надо заранее продумать последовательность gRNA, чтобы она вела Cas9 к нужному месту в геноме, а не куда-нибудь еще. Если мы идем по пути HDR, то также надо продумать последовательность донора. Кроме того, надо спланировать, как и в каком виде мы будем доставлять все это в клетки – тут есть разные варианты в зависимости от кучи факторов (тип клеток, размер вставки и т.п.). Наконец, последняя часть эксперимента самая нудная – нам надо отсортировать клетки, в которых ничего не поменялось (клетки дикого типа), от тех, где мутация произошла! Тут у ученых тоже имеется целый арсенал методов, от простых на основе ПЦР, типа GCD (Genomic Cleavage Detection), до полногеномного секвенирования на монстроподобных агрегатах.
Надеюсь, мне удалось простым языком объяснить, что же такое CRISPR, и как его применяют! В качестве бонуса фотка меня пару лет назад, когда мне удалось лично познакомиться с применением технологии CRISPR.
Эти зеленые клеточки на экране микроскопа еще вчера были синими, но потом пришел автор и с помощью протокола HDR внедрил однонуклеотидную замену в ген BFP, превратив его в GFP.
Спасибо, что прочитали! До встречи в новых постах!
Методика редактирования генов с помощью CRISPR/CAS9
Новая озвучка. Анимационный ролик 2014 года о методике редактирования генов CRISPR/CAS9 о которой слышали, наверное, все.
На сегодняшний день методика уже сильно развилась, но в данном ролике речь идёт о базовых вещах, в рамках школьной биологии, без лютой биохимии, и информация вполне актуальна.
Сейчас методика практически достигла своего предела применения, основная, пока не решаемая проблема, – это далеко не идеальная избирательность: вероятность действия комплекса на участки ДНК, отличающиеся от гидовой РНК на один или несколько нуклеотидов, очень высокая. Случайные мутации, нам, естественно, ни к чему… хотя зависит от ситуации, если у нас задача вывести ГМО мышек, то вполне можно забить и отобрать относительно здоровые особи. Но о применении к человеку, особенно в эмбриональном периоде и речи быть не может.
И мы упомянули в видео PAM последовательность (Protospacer adjacent motif) – это важная фишка, в природе это последовательности всего из нескольких нуклеотидов (они находятся на краю встроенного вирусом участка) к которым изначально присоединяется CRISPR/CAS9 комплекс, и только после этого он начинает проверку на совпадение с гидовой РНК, строго проверяется всего только 6-12 нуклеотидов, а дальше уже допускаются отклонения. В природе такие отклонения оправданы, таким образом заодно вырезаются уже успевшие немного мутировать (на парочку незначительных нуклеотидов) вирусные последовательности, но в лаборатории это вызывает проблемы, описанные в предыдущем абзаце.
Не вижу смысла расписывать здесь что-то более подробно, это уже много раз сделано в других местах, например, прекрасная статья с картинками, для тех, кто хочет поподробнее: https://biomolecula.ru/articles/prosto-o-slozhnom-crispr-cas
Перевод и озвучка мои.
Оригинал видео и доп. информация (англ.): https://www.youtube.com/watch?v=2pp17E4E-O8
Музыка: Asher Fulero – Renunciation.
Топ лучших вопросов недели: про бессонницу, тупость и ремонт
— Что делать, если я очень тупая?
— Как спать всю ночь не просыпаясь?
— Правда ли, что женщины в 40+ не хотят детей и семью?
— Откуда берется кредитная история?
— Что делать, если отказывают в гарантийном ремонте?
— Реально ли сделать ремонт самостоятельно?
— Какую машину купить до 500к?
По традиции на вопросы сотни отборных ответов в лента Экспертов ➔



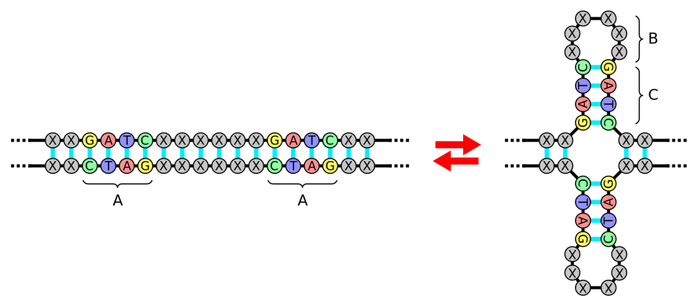
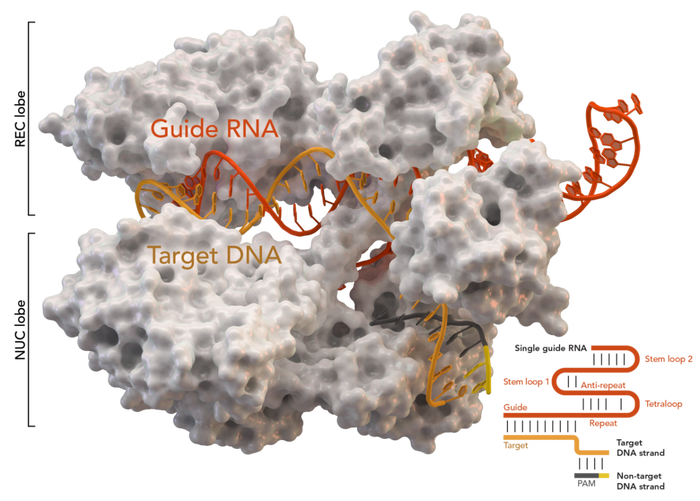
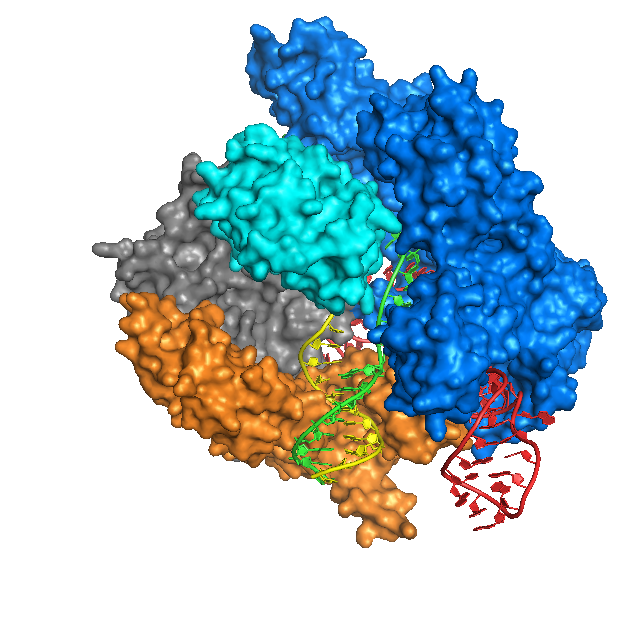

![CRISPR/Cas9 [научный фотоконкурс] Научный фотоконкурс, Crispr-cas9, Биохимия, Длиннопост](https://cs13.pikabu.ru/post_img/2020/12/07/0/1607289149140475731.jpg)
![CRISPR/Cas9 [научный фотоконкурс] Научный фотоконкурс, Crispr-cas9, Биохимия, Длиннопост](https://cs13.pikabu.ru/post_img/2020/12/07/0/1607289173115256580.jpg)
![CRISPR/Cas9 [научный фотоконкурс] Научный фотоконкурс, Crispr-cas9, Биохимия, Длиннопост](https://cs10.pikabu.ru/post_img/2020/12/07/0/160728929414548059.jpg)