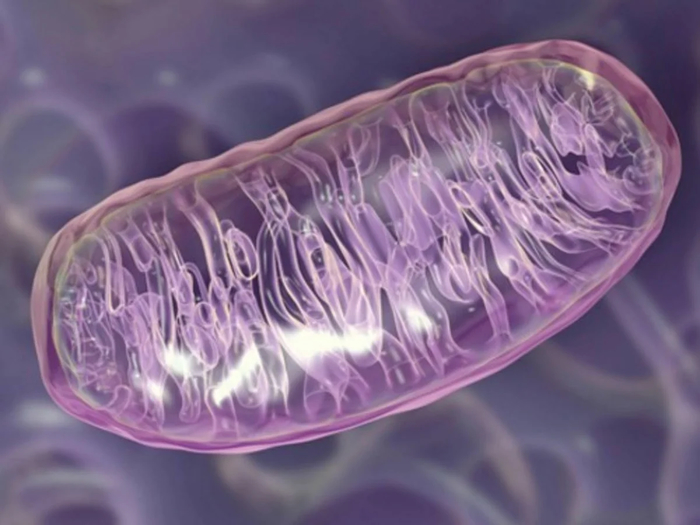
Иные Митохондрии
Этот пост про создание возможности дыхания организма, кроме кислорода и другими газами.
Митохондрии наше всё.
Бактерия в далёкие времена поселившаяся в животной клетке стала её симбионтом и обеспечила выживание животных организмом в кислородный среде. Вероятно без них и не была бы возможна жизнь многоклеточных животных организмов.
Что делает митохондрия:
Вкратце митохондрии производят АТФ используя в виде топливных молекул кислород забирая у молекул кислорода электронны.
Представьте себе если учёные выведут бактерии которые, наподобие митохондрии, могут использовать в виде топливных молекул иные молекулы вместо кислорода. Возможно не только простых молекул но и сложных.
И внедрят их в клетки организма в которых они будут сосуществовать вместе с митохондриями и начинать выполнять функцию выработки АТФ при попадании организма в чужеродную среду.
Почему это представляется возможным? : так это потому, что митохондрии от кислорода нужен только электрон, который она умеет у него забирать. А если создать органеллу которая способна брать электрон у других веществ.
Представьте себе что будут созданы такие органелы для различных сред, и будут переключаться при попадания в неблагоприятные (иные) условия.
Представьте себе в таком случае организм бы мог обходится и без скафандра в чужеродной атмосфере. И яды бы были не почем...
Вы хотите головоломок?
Их есть у нас! Красивая карта, целых три уровня и много жителей, которых надо осчастливить быстрым интернетом. Для этого придется немножко подумать, но оно того стоит: ведь тем, кто дойдет до конца, выдадим красивую награду в профиль!
Как повысить выносливость? делюсь научными данными и свои опытом
Начнем с такого вопроса, что же такое выносливость? Это способность человека продолжительно выполнять работу без признаков утомления и быстро восстанавливаться.
Что отвечает у нас в организме за выносливость? Количество митохондрий в наших клетках. Во время выполнения упражнений вырабатывается молочная кислота, ее количество зависит от интенсивности упражнения, наши митохондрии начинают сжигать молочную кислоту ,но если их количество мало, то мы начинаем терять работоспособность, и молочная кислота остается накапливаться. Следовательно, делаем вывод чем больше митохондрий, тем лучше у нас выносливость.
О митохондриях
Митохондрия - это часть наших клеток, которая отвечает за выработку энергии для этих клеток. Она превращает глюкозу и жиры из пищи в энергию. Больше всего в организме митохондрии крепятся на окислительных мышечных волокнах или как еще их принято называть медленные волокна. Чем больше окислительных волокон, тем больше можно накопить митохондрий.
Методы накопления митохондрий
Возьмем в пример бег. Выполняем ускорения от 6 до 15 секунд, примерно 80-90% от максимальной скорости. После каждого подхода делаем 2 минуты отдыха до полного восстановления. 10 подходов тонизирующий вариант, от 20 подходов и более развивающий.
В другом режиме делаем ускорения примерно около 40-50 секунд, 70-80% от максимума. Здесь уже отдыхаем около 4-5 минут до полного восстановления. Количество подходов от 3 до 7 по самочувствию.
Итог выше написанного
Давайте тренироваться по науке, сколько можно пахать и умирать на тренировках, а результата нет, попробуйте эту программу, взял ее из трудов В.Н. Селуянова, чувствую себя намного лучше и результаты выросли почти во всех упражнениях. Так же можно подбирать эту схему под любые упражнения, в зависимости в какой группе мышц мы хотим развивать выносливость. Если понравилась статья ставьте лайки и обязательно давайте обсудим в комментариях, что непонятно и все разберем и дополним. В следующей статье расскажу о двух других методах, подписывайся на канал, чтобы ничего не пропустить. Всем благ и упорства!
Телеграм канал Позволь себе расти
Предки митохондрий были паразитами?
Митохондрии - это эукариотические органеллы, которые когда-то давно были бактериями.
Конечно кто-то может возразить, что это всего лишь гипотеза, однако эта гипотеза уже давно переросла в эндосимбиотическую теорию и является общепринятой в кругах учёных. Так уже давно считается, что митохондрии произошли когда-то от альфа-протеобактерий, вероятно, два миллиарда лет назад. Но, остается неясным, что составляло начальный эндосимбиоз между альфа-протеобактерией и ее хозяином. В частности, какую роль сыграл митохондриальный предок, инициировавший эндосимбиоз? В связи с этим вопросом возникают и другие. Например:
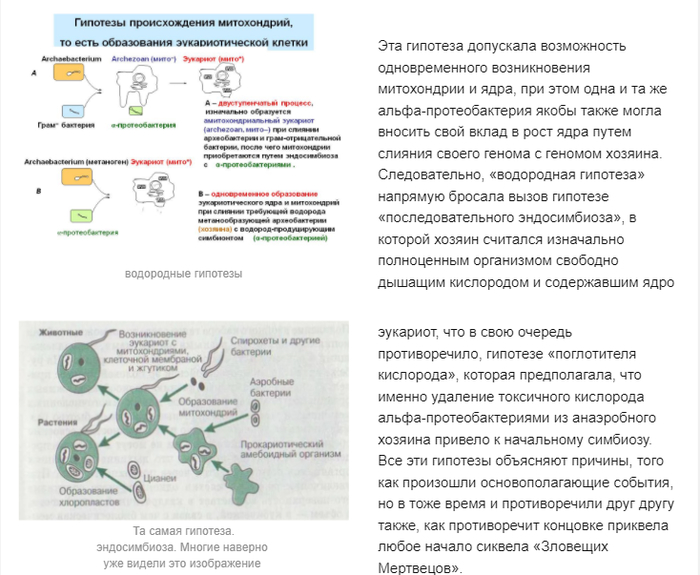
Для объяснения всех обстоятельств и ответов на все вопросы, связанные с основными эндосимбиотическими событиями, выдвигались разные гипотезы зачастую противоречащие друг другу. Так, например, «Водородная гипотеза» предполагала метаболическую синтрофию между водорода-продуцирующими альфа-протеобактериями и водорода-зависимыми археонами, как движущую силу эндосимбиоза.
В связи с этим в последнее время стала набирать ещё одна гипотеза возникновения митохондрий, которая рассказывает нам о паразитических предках митохондриях. Эта гипотеза на данный момент кажется является более достоверной, так как подкрепляется большим количеством данных. Так в 2020 году вышло огромное филогенетическое исследование показывающее близкое родство митохондрий с паразитическими бактериями. [1]
Но не менее интересное исследование, с которого всё и началось, произошло в 2014 году [2].
Хотя мне следует чуть-чуть поправить себя, так как предположения о митохондриях-паразитах высказывались не однократно и ранее, но именно это исследование можно назвать самым крутым и начальной «точкой отсчёта» к последующим событиям в научной среде. Поэтому сегодня именно его я и буду рассматривать.
А всё началось как раз с реконструкции митохондриального предка, который имеет большое влияние на наше понимание происхождения митохондрий. Так все выше описанные мной гипотезы объяснялись исследованиями, которые в основном были сосредоточены на реконструкции последнего общего предка всех современных митохондрий, так называемых прото-митохондрий, но не основывались на более информативных премитохондриях, которые по сути были ещё древнее прото-митохондрии, так как они включали последнего общего предка как митохондрий, так и их сестринской клады альфа-протеобактерий.
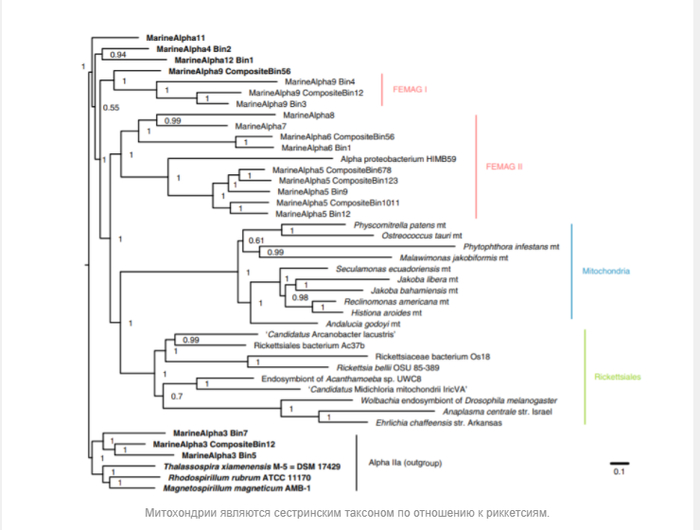
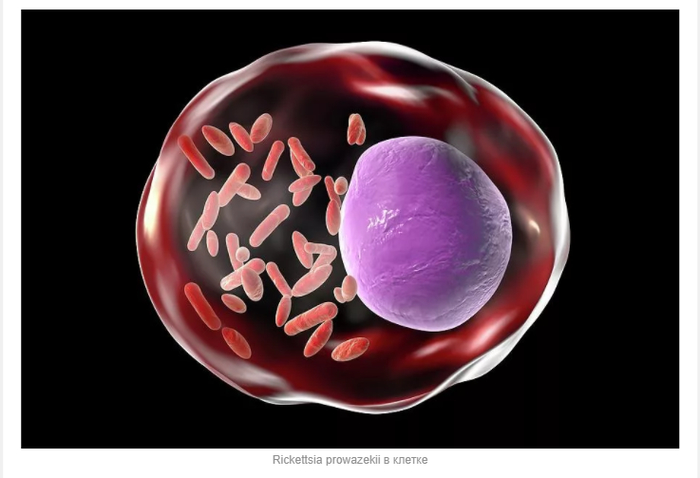
Самые известные из них это вольбахии и риккетсиалы (отряд в который входят риккетсии). Последние нас интересуют больше всего, так как именно они успели поучаствовать в реконструкции предка митохондрий, а точнее их метаболизма в 2014-м году.
Так, чтобы получить представление об обстоятельствах, которые окружали начальное событие эндосимбиоза, учёные старательно реконструировали метаболизм прото-митохондрий и премитохондрий. Для этого они сначала восстанавливали прото-митохондриальные гены, которые в процессе эволюции были потеряны для ядра. Учёные назвали эти гены ядерными генами митохондрий. Восстановление этих генов являлось предпосылкой для реконструкции митохондриальных предков. Предыдущие попытки найти прото-митохондриальные гены были безуспешны так как основывались на довольно ограниченной доступности бактериальных и эукариотических геномов на момент их изучения [3;4].
Используя значительно увеличившееся представление геномов эукариот и альфа-протеобактерий, исследователи провели филогеномный анализ для систематической идентификации ядерных генов, происходящих из митохондрий. Гены эукариот с наибольшим попаданием в BLAST митохондрий / альфа-протеобактерий сначала были объединены в группы генов. Филогенетическое дерево было реконструировано для каждого семейства, и ядерные гены, которые сгруппировались с альфа-протеобактериями на деревьях, были идентифицированы как происходящие из митохондрий.
Начав с 427186 генов из 30 эукариотических геномов, представляющих широкий диапазон филогенетического разнообразия, они идентифицировали 4459 генов, принадлежащих к 394 семействам, как ядерные гены митохондрий. Чтобы исключить недавний перенос генов, специфичных для клонов, между альфа-протеобактериями и эукариотами, генные семейства должны были присутствовать по крайней мере в двух альфа-протеобактериальных и двух эукариотических линиях. Собственно, так и произошло. Таким образом учёные смогли идентифицировать, что ядерные гены из 394 семейств присутствуют в прото-митохондриях.
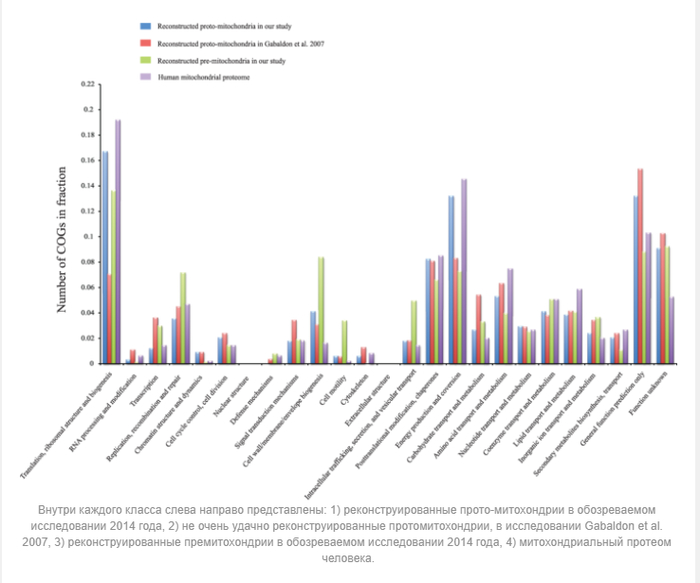
Всё это есть и в современных митохондриях. Однако учёные обнаружили и то, чего в прото-митохондриях не было. Так в них отсутствовали функциональные категории, такие как репликация ДНК и транскрипция, также в значительной степени отсутствовали в реконструированном метаболизме и гетеротрофные углеводные обмены, такие как гликолиз и пентозофосфатный путь. Таким образом реконструкция прото-митохондрии показала упрощённого предка митохондрии более похожего на современную митохондрию, что опровергло предыдущие гипотезы о ближайших предках митохондрий, которые имели огромное множество разнообразных функций.
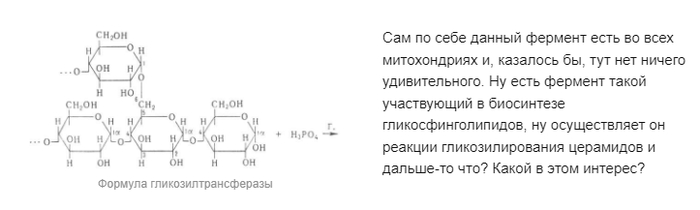
При дальнейшем изучении уже самих митохондрий учёные по-новому взглянули на метаболизм эукариот, происходящий главным образом благодаря этим органеллам. Особый интерес представлял ряд генов, участвующих в метаболизме липидов эукариот. Были идентифицированы несколько генов, участвующих в биосинтезе нуклеотидов de novo, как происходящих из митохондрий. Обнаружены были и ферменты, участвующие в биосинтезе стероидов предполагающие, что митохондриальный предок внес свой вклад в биосинтез оных. Вишенкой на торте можно назвать идентификацию церамидгликозилтрансферазы (COG1215).
А интересно то, что этот фермент расположенный на «ассоциированной с митохондриями мембране», специфическом субдомене ER, который связывает этот самый ER и митохондрии, обнаружился и в риккетсиях. Для понимания замечу, что все эти самые гликосфинголипидные, и церамидные структуры, повсеместно присутствуют в качестве важных мембранных компонентов почти во всех эукариотических клетках и митохондриях, а это в свою очередь говорит нам о том, что присутствие этих структур в бактериях являются крайне редкими. При этом, что интересно, ген отвечающий за все эти субстраты и гликолипидные продукты, присутствующий в бактериальных клетках всё же различается от эукариотических гликозилтрансфераз. Следовательно, данный факт указывает на бактериальное происхождение этого гена, который был приобретён эукариотами для новой функции по синтезу собственных эндомембран, а также по перекрестному взаимодействию и перемещению липидов между митохондриями и субодменом ER. Интересные результаты не так ли?
В результате получилось, что митохондрии поместились в отряд к риккетсиалам в качестве сестринской клады по отношению к семействам Rickettsiaceae, Anaplasmataceae и Candidatus Midichloriaceae, которую в свою очередь были подчинены семейству Holosporaceae.
Стоит отметить, что представители этих семейств являются паразитами. Так, учёные в этой работе показали, что все пять линий секвенированных риккетсиалов тесно связаны с митохондриями. Далее основываясь на приблизительной линейной зависимости между числом семейств генов, средним числом генов и размером генома учёные заметили, что геном премитохондрий сокращался. Это типично для облигатной внутриклеточной бактерии и предполагает, что сокращение генома шло полным ходом до того, как митохондрии отделились от альфа-протеобактерий, т. е. стали настоящими митохондриями.
Продолжив генетические исследования, учёные стали сравнивать реконструированные прото-митохондрии и премитохондрии. Оказалось, что в отличии узкоспециализированных прото-митохондрий, премитохондрии были способны к гораздо более разнообразному метаболизму. Помимо основных путей, премитохондрии участвовали в трансляции, в клеточной стенке, LPS и биогенезе мембран, в производстве энергии, репликации, рекомбинации и репарации ДНК, они обладали множеством ключевых метаболических путей, включая гликолиз, цикл TCA, пентозофосфатный путь и путь биосинтеза жирных кислот. Кроме того, премитохондрии обладали большим количеством генов, участвующих в синтезе различных кофакторов, таких как рибофлавин, фолат, биотин и убихинон.
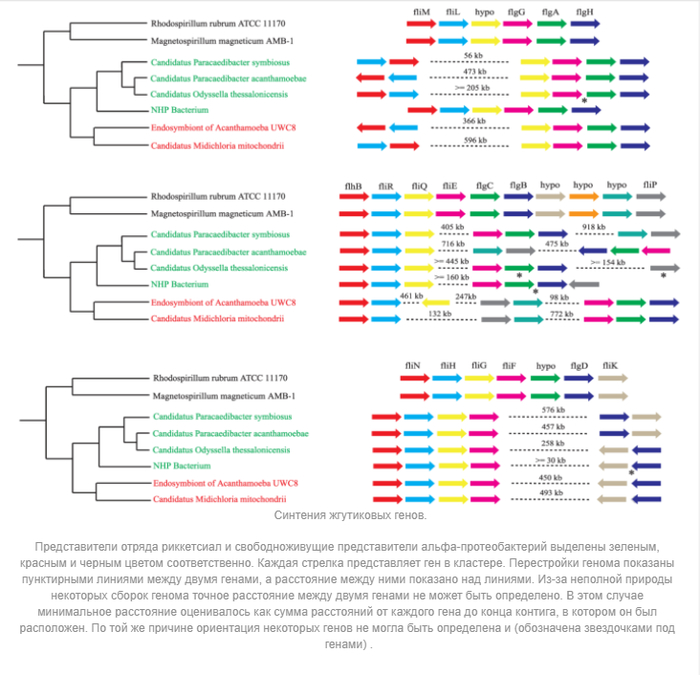
Дальнейшие исследования премитохондрий показали, что они кодируют пластидно-паразитарный тип транслоказы АТФ / АДФ, которая импортирует АТФ от хозяина, что делает премитохондрию энергетическим паразитом. Последующие сравнения генов риккетсиалов с премитохондриями, а также построения филогенетических деревьев показало, что премитохондрии вероятно обладали способностью дышать в условиях низкого содержания кислорода и имели жгутики, которые наследовались вертикально, а не через горизонтальный перенос. Электронная микроскопия части эндосимбиотических бактерий также показала наличие рудиментарных жгутиков. Т.е. данное исследование показывает нам предка митохондрии, который мог жить в условиях с низким содержанием кислорода, обладающим жгутиком и являющимся паразитом, что, казалось бы, прямо контрастирует с нынешней ролью митохондрий как производителя энергии клетки.
Однако, систематический обзор от 2011 года бактериального симбиоза показал, что мутуализмы вполне себе могут происходить либо непосредственно от свободноживущих бактерий в окружающей среде, либо от внутриклеточных паразитов [5]. Ключевое различие между этими двумя эволюционными путями состоит в том, что для инициации симбиоза свободноживущие бактерии должны приносить немедленную пользу хозяину, в то время как внутриклеточные паразитические бактерии этого не делают.
Вместо опровержения прошлых предположений данная гипотеза предлагает применять их для объяснения перехода митохондрий от паразита к мутуалистической органелле на более поздней стадии. Это всё очень интересно, а потому есть большая вероятность, что гипотеза о предках митохондриях как паразитах возможно скоро станет научной теорией. Поэтому если, кто-то назовёт Вас паразитом, не обижайтесь, ведь можно парировать, что паразитизм у нас в крови, а точнее в клетках. Такие дела!
Автор: биолог, вдохновитель научного сообщества Фанерозой, Ефимов Самир
Оригиналы: Публикация фанерозойских материалов на платформе "Вконтакте", "Хабр" и "Пикабу".
1. «Phylogenetic analyses with systematic taxon sampling show that mitochondria branch within Alphaproteobacteria» Lu Fan, Dingfeng Wu, Vadim Goremykin, Jing Xiao, Yanbing Xu, Sriram Garg, Chuanlun Zhang, William F. Martin and Ruixin Zhu; Nature Ecology & Evolution, 2020
2. Phylogenomic Reconstruction Indicates Mitochondrial Ancestor Was an Energy Parasite Zhang Wang, Martin Wu Published: October 15, 2014Gabaldon T, Huynen MA (2003) Reconstruction of the proto-mitochondrial metabolism. Science 301: 609.
3. Gabaldon T, Huynen MA (2007) From endosymbiont to host-controlled organelle: the hijacking of mitochondrial protein synthesis and metabolism. PLoS Comput Biol 3: e219.
4. Gabaldon T, Huynen MA (2007) From endosymbiont to host-controlled organelle: the hijacking of mitochondrial protein synthesis and metabolism. PLoS Comput Biol 3: e219.
5. Sachs JL, Skophammer RG, Regus JU (2011) Evolutionary transitions in bacterial symbiosis. Proc Natl Acad Sci U S A 108 Suppl 210800–10807.
Третий не лишний. Зачем ребенку дополнительный родитель?
Недавно мир облетела новость: родился первый в мире «ребенок от трех родителей». Однако уже в этом августе методика, которая должна была решить проблему наследственных заболеваний, была запрещена в США. Мы разобрались, зачем и кому нужна эта технология, почему она встречает сопротивление, да и первый ли это ребенок с третьим родителем?
Папа, мама… и митохондрия
Ребенок появился на свет 6 апреля 2016 года в Мексике. Его мать – носительница редкой генетической мутации, которая при естественном оплодотворении может привести к развитию у ребенка синдрома Лея. Это смертельное расстройство, поражающее нервную систему, и лечить его пока не научились. Гены, мутация которых вызывает заболевание, находятся не в ядрах клеток, где расположена большая часть генетического материала, а в митохондриях – особых компонентах клетки – органеллах, находящихся в ее цитоплазме и имеющих свой геном. А, как известно, митохондрии нам достаются только от матери, те, что содержатся в яйцеклетке.
Сама мать ребенка здорова, но около четверти ее митохондрий имеют болезнетворную мутацию, по вине которой женщина пережила четыре выкидыша и потеряла двух своих предыдущих детей в возрасте 8 месяцев и 6 лет. Новая методика позволила ей родить здорового мальчика. Он унаследовал ДНК от трех человек – своих родителей – и митохондриальную ДНК женщины-донора. Но обо всем по порядку.
Что же такое митохондрии и почему они имеют свой геном? На самом деле они есть не только в материнской яйцеклетке, но и в сперматозоидах. В них они обеспечивают активность и подвижность на пути к яйцеклетке. Однако после слияния сперматозоида с яйцеклеткой происходит их гибель. Собственно, они есть практически во всех клетках организма. Митохондрия – это энергетическая станция клетки.
Строение клетки / © wikimedia.org
Их основная функция – окисление органических соединений и использование освобождающейся при их распаде энергии для генерации электрического потенциала. Митохондрии синтезируют АТФ – аденозинтрифосфат – универсальную форму химической энергии в любой живой клетке, проще говоря, топливо для наших клеток.
Число митохондрий в клетке непостоянно. Особенно много их в клетках, в которых велика потребность в кислороде. Мозг, сердце, мышцы – в их клетках содержатся сотни и даже тысячи митохондрий. Впервые митохондрии были обнаружены в 1850 году именно в мышечных клетках. Всего митохондриальная ДНК содержит 37 генов – 13 кодируют белки, 22 – гены тРНК, 2 – рРНК. Это гораздо меньше общего количества генов в геноме человека. В настоящее время предполагается, что геном человека содержит от 20 000 до 25 000 генов. Тем самым количество митохондриальных генов у нас незначительно, чего не скажешь об их значении.
Есть не так много организмов, которые могут обходиться без митохондрий. Митохондрии присутствуют в клетках растений и животных. Тем более удивительно понимать, что в наших клетках они чужаки.
Митохондрии «живут с нами» почти 2,4 миллиарда лет. Это тогда, во время кислородной катастрофы, наши, еще одноклеточные и безъядерные, предки (прокариоты) «приручили» бактерий, способных использовать кислород для генерации энергии. Бактерии, предки наших митохондрий, поселились внутри клеток и позволили им приспособиться к глобальному изменению состава атмосферы. Возросшее содержание свободного кислорода в ней оказалось губительно для подавляющей части организмов того времени.
В процессе такого симбиоза некогда самостоятельные предки митохондрий передали большинство своих генов сформировавшемуся ядру теперь уже ядерных клеток (эукариот). Себе они оставили только часть своего прежнего генома. Причем данный скачок эволюции произошел в том числе и благодаря возросшей энергоэффективности клетки. Подобное, как говорят ученые, симбиотическое происхождение имеют не только митохондрии, но и, например, хлоропласты, также имеющие свою ДНК.
Современным примером подобного симбиоза может служить Elysia chlorotica – небольшой морской слизень, относящийся к брюхоногим моллюскам, который буквально на глазах превращается в фотосинтезирующее животное.
Гены, как известно, могут подвергаться мутациям. По разным причинам мутации в митохондриальной ДНК происходят намного чаще, чем в ядерной. Следствие этому – митохондриальные заболевания. А иногда темп мутирования в митохондриальной ДНК увеличивается еще и из-за мутаций в ядерных генах, которые кодируют ферменты, контролирующие репликацию ДНК митохондрий.
Митохондриальные заболевания приводят к нарушениям энергетических функций в клетках различных органов человека. Синдром Лея был описан еще в 1951 году британским нейропсихиатром Арчибальдом Денисом Леем. Дети, рождающиеся с этим синдромом, никогда не доживают до совершеннолетия, а обычно погибают уже в возрасте нескольких лет. Заболевание поражает и мозг, и мышцы. В среднем, этот синдром поражает одного выжившего новорожденного из 40 000. Но в некоторых регионах этот показатель значительно выше. Например, в районе Сагеней-Лак-Сен-Жан, что в центральном Квебеке (Канада), болен один ребенок из 2000 новорожденных.
Он был первый?
Ребенок, родившийся прошлой весной в Мексике, получил имя Абрагим Хассан. Его родители – супружеская пара из Иордании. Завести здоровых детей они не могли на протяжении почти 20 лет. Осуществить мечту им помогла команда эмбриологов из Нью-Йоркского Центра оплодотворения «Новая надежда» (New Hope Fertility Centre) во главе с доктором Джоном Чжаном (John Zhang).
В действительности Чжан не первый, кто объединил ДНК трех человек в одном эмбрионе. В 90-х годах прошлого столетия несколько клиник в США уже проводили подобные процедуры. Разработанный американским ученым Жаком Коэном метод цитоплазматической замены позволил появиться от 30 до 50 детям, у которых есть «три родителя». Имена некоторых детей даже стали известны. Например, Алана Сааринен, которая была зачата в США в рамках эксперимента по лечению бесплодия.
Алана Сааринен / ©bbc.com
Но затем вмешалось FDA (Food and Drug Administration) – Управление по контролю за продуктами и лекарствами – и запретило его применение как из-за этических вопросов, так и из-за соображений безопасности. Этот метод был относительно прост, но имел существенный недостаток. Он предполагал инъекцию цитоплазмы женщины донора в яйцеклетку будущей матери. Но в этом случае дефектные митохондрии матери не удаляются из цитоплазмы, а только дополняются здоровыми митохондриями донора. В клетке ребенка образуется смесь разных митохондрий, как здоровых так и больных. При дальнейшем делении клетки они распределяются случайным образом, и есть вероятность, что дефектные материнские митохондрии могут вновь перевесить числом здоровые донорские, а это приведет к развитию болезни. По некоторым сведениям, у части детей были развиты генетические нарушения.
Заслуга Чжана в том, что родившийся в прошлом году ребенок появился на свет благодаря новой технологии. Она называется «перенос материнского веретена». Он взял ядро из яйцеклетки матери и переместил его в донорскую яйцеклетку, собственное ядро которой было предварительно удалено. Полученная яйцеклетка с ядерной ДНК от матери и митохондриальной ДНК от донора затем оплодотворялось спермой отца. Такая техника должна позволить полностью избежать переноса материнских митохондрий. Команда Чжана использовала этот подход для создания пяти эмбрионов, и только один из них развился благополучно. Этот эмбрион был введен в полость матки женщины, и уже девять месяцев спустя родился ребенок. Подобные процедуры во многом повторяют технологию экстракорпорального оплодотворения (ЭКО), когда само оплодотворение происходит вне организма женщины («в пробирке»).
Две методики современной митохондриальной терапии / © nature.com
Манипуляции с клетками команда Чжана провела в Нью-Йорке. После оплодотворения эмбрионы были отправлены в Мексику, чтобы там имплантировать их в матку матери. Процедура была проведена в больнице в Мексике, так как в США подобные процедуры не разрешены, а к югу от Рио-Гранде в этой сфере существует правовой вакуум.
Другой метод, уже одобренный в Великобритании, носит название «пронуклеарный перенос» и включает оплодотворение как яйца матери, так и донорского яйца спермой отца. Прежде чем оплодотворенные яйца начнут делиться, каждое ядро удаляется. Ядро из оплодотворенной яйцеклетки донора удаляется и заменяется ядром из оплодотворенной яйцеклетки матери. Но для семейной пары из Иордании такой метод был неприемлем, так как они были против уничтожения эмбрионов.
Между запретом и разрешением
У Джона Чжана были большие планы относительно своей методики. Он хотел использовать ее не только для защиты эмбриона от наследственных заболеваний, но и для решения проблемы возрастного бесплодия. После успешного рождения здорового ребенка Чжан создал компанию Darwin Life, которая должна была помочь женщинам старше 40 испытать радость материнства. Одна такая процедура обошлась бы клиентам в $80 000–120 000.
Доктор Джон Чжан и родившийся ребенок с «тремя родителями» / © newscientist.com
Однако 4 августа FDA (Food and Drug Administration) отправило доктору письмо с требованием прекратить рекламировать примененную им процедуру. В своем письме FDA напомнило доктору, что не давало разрешение на такие манипуляции.
В апреле прошлого года Чжан запросил у FDA разрешение на проведение клинических испытаний. Однако FDA запрещает модифицировать эмбрион человека, если допускается его последующее развитие. Кроме того, экспериментальная процедура не считается полностью безопасной. Родившийся мальчик еще не вырос, и пока неясно, как эксперимент повлияет на его здоровье в будущем. Но, несмотря на отсутствие клинических испытаний, Чжан активно продвигает свою методику и обещает восстановить утраченную с возрастом фертильность. Именно этот факт возмутил FDA.
Единственной страной в мире, где разрешено искусственное оплодотворение с ДНК от трех родителей, является Великобритания. В феврале 2015 года Палата общин Британского парламента большинством голосов разрешила донорство митохондрий при искусственном оплодотворении. Но порядок применения таких процедур и требования к получению клиниками разрешений на его применение появились только в декабре прошлого года, когда британский комитет по рождаемости и эмбриологии (Human Fertilisation and Embryology Authority) начал прием заявок от больниц. Возможность воспользоваться процедурой будет только у женщин, имеющих очень высокий риск рождения ребенка с угрожающим жизни митохондриальным заболеванием. Первыми лицензии планируют получить медики из Университета Ньюкасла, где был разработан этот метод терапии. Процедуры должны были начаться весной этого года, и первые британцы с «тремя родителями» должны родиться до конца 2017 года.
США также стоят на пороге легализации процедуры. В феврале прошлого года Комитет по вопросам этической и социальной политики направил в FDA доклад, посвященный новым методам предотвращения передачи материнских заболеваний c митохондриальной ДНК. Его рекомендации, вероятно, станут официальной политикой американского регулятора.
Возможно, первыми детьми с донорскими митохондриями будут исключительно мальчики. Это ограничение будет сделано специально, чтобы исключить передачу донорской митохондриальной ДНК по наследству следующему поколению. Дети с тремя родителями будут, а детей с тремя бабушками – пока нет.
Тем самым, если применение методики будет иметь негативные последствия, то они отразятся только на родившихся детях и не передадутся их будущему потомству.
Между тем, несмотря на то, что новые методики позволяют решить проблемы многих семей и их, хоть и с опаской, но начинают разрешать контролирующие органы, у них есть и противники с этическими аргументами. Редактирование генома человека делает нас на шаг ближе к потребительской евгенике, считает доктор Дэвид Кинг, молекулярный биолог и основатель общественной группы Human Genetics Alert. «В свое время благодаря безответственному поведению научного сообщества, а также с очевидной гонкой за славой и прибылью, мы позволили появиться генномодифицированным продуктам, теперь, похоже, пришло время проводить кампанию за глобальный запрет на генную инженерию людей, –говорит Кинг. – Когда вы начинаете создавать общество, в котором дети богатых людей получают биологические преимущества перед другими детьми, основные понятия человеческого равенства теряются. Вместо этого вы получаете социальное неравенство, записанное в генах».