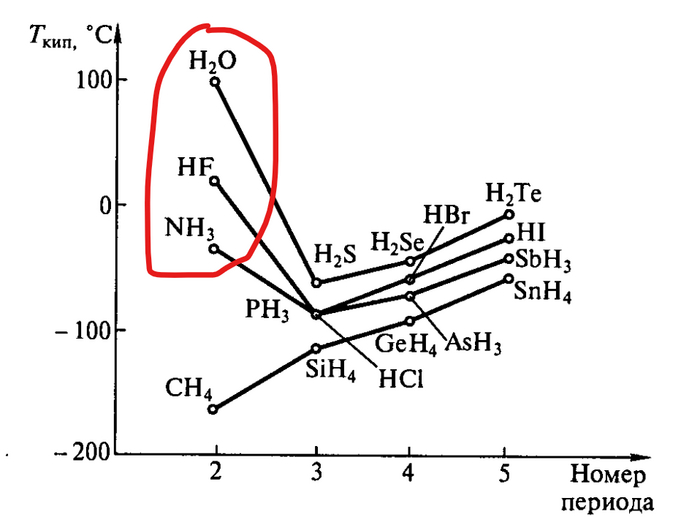
Водородные связи, по мнению школьного учебника, всего лишь сильная версия межмолекулярных связей, между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом, которые делают воду жидкой при 20 градусах, а не газом, ну и другие вещества заодно, например аммиак, фтороводород и т.д.
Если же вы спросите химика, что такое водородная связь без упрощений, такого простого ответа вы не дождетесь. Водородная связь берет свою устойчивость как из электростатических сил кулона, из ковалентных взаимодействий между молекулами, так еще из поляризаций молекул друг дружкой т.е. всё очень сложно.
Подобная сложность описания водородной связи кидает свою тень на кучу разделов химии, биологии, материаловедения и физики, например спектры поглощения и рассеивания для воды и водяного пара, чрезвычайно сложно получить теоретически (никто не смог пока что), как раз всё портят водородные связи, ученые до сих пор спорят, какую модель лучше развивать для описания этого спектра.
У химиков водородные связи попали в зазор между классическими моделями химических взаимодействий (ковалентные, межмолекулярные, электростатические) прям как герой Тома Хэнкса из фильма "Терминал", который застрял в аэропорту, ибо не имел никакого гражданства и никто не хотел его принимать. Приходится либо подключать квантовую механику для описания, либо пользоваться эмпирическими расчетами (подгонометрия), либо и тем и другим одновременно (охохо...)
А вот самая главная жертва этого всего, это молекулярная биология. Практически всё и вся там может связываться друг с другом водородными связями. Поэтому белки определяют свою форму и функцию, химические реакций выбирают путь учитывая водородные связи...
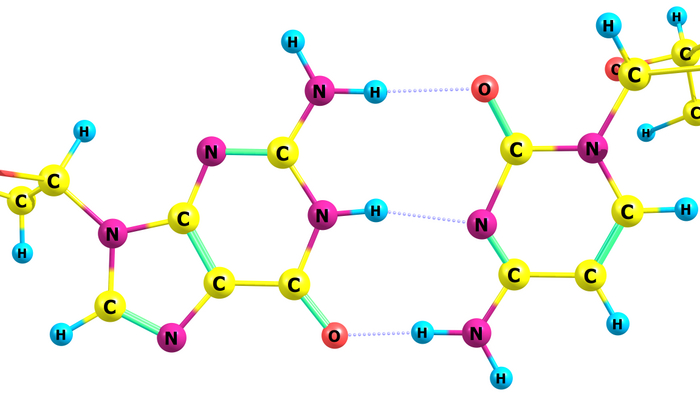
Водородные связи между гуанином и цитозином в молекуле ДНК или РНК